PEDRO VILLALBA APESTEGUI1, SANTIAGO NAVA2, JULIA BRIGNONE3, CARINA SEN3, AMADEO ESPOSTO4, VIRGINIA ANGELETTI4
1Servicio de Infectología, Hospital Escuela de Agudos Dr. Ramón Madariaga, Posadas, Misiones, 2Laboratorio de Parasitología e Inmunología, Instituto Nacional de Tecnología Agropecuaria, Estación Experimental Agropecuaria Rafaela, Santa Fe, 3Departamento Diagnóstico Laboratorial y Referencial, Instituto Nacional de Enfermedades Virales Humanas Dr. Julio I. Maiztegui, Pergamino, Buenos Aires, 4Servicio de Infectología, Hospital Interzonal General de Agudos General San Martin, La Plata, Buenos Aires, Argentina
Resumen Se comunica un caso autóctono de fiebre manchada por Rickettsia parkeri en un adulto residente en Ensenada, Provincia de Buenos Aires ocurrido en el verano de 2016. El cuadro, secundario a una mordedura de garrapata en la pierna izquierda, se presentó como un síndrome febril agudo con deterioro del estado general, cefalea, mialgias, artralgias y exantema maculopapular. El sitio de la mordedura presentaba una úlcera con escara necrótica. El diagnóstico se confirmó por conversión serológica IgG anti-antígenos del género Rikettsia. La secuencia de un fragmento del gen gltA amplificado a partir de la lesión de piel presentó 100% identidad nucleotídica con las secuencias de cepas de R. parkeri aisladas en Argentina y en varios países de América. El paciente evolucionó favorablemente al tratamiento con doxiciclina.
Palabras clave: rickettsiosis, fiebre manchada, Rickettsia parkeri, enfermedades transmitidas por garrapatas, Argentina
Abstract
Autochthonous case of spotted fever caused by Rickettsia parkeri in Ensenada, Buenos Aires.
We present a case of spotted fever occurred in an adult residing in Ensenada, Buenos Aires province in February 2016. The patient presented with an acute febrile syndrome associated with a skin necrotic lesion on the left leg secondary to a tick bite. The general symptoms were a maculopapular rash, headache, myalgia, and arthralgias. Seroconversion of anti-Rickettsia specific IgG antibodies confirmed recent infection. The nucleotidic and aminoacidic sequences of a gltA gen fragment matched 100% the sequences of R. parkeri strains from Argentina and other countries of America. The patient responded well to treatment with doxycycline.
Key words: Rickettsia infections, spotted fever, Rickettsia parkeri, tick-borne diseases, Argentina
Recibido: 25-XI-2016 Aceptado: 14-III-2018
Dirección postal: Dr. Pedro A. Villalba Apestegui, Servicio de Infectología, Hospital Escuela de Agudos Dr. Ramón Madariaga, Av. Marconi 3736, 3300 Posadas, Misiones, Argentina
pedroandresvillalba@gmail.com
Las fiebres manchadas constituyen un grupo de zoonosis causadas por bacterias intracelulares del género Rickettsia transmitidas por garrapatas. En Argentina se han registrado casos humanos por R. rickettsii en la provincia de Jujuy y por R. parkeri en las provincias de Córdoba, San Luis, La Rioja y Buenos Aires, entre otras1. Describimos aquí un caso autóctono de rickettsiosis por R. parkeri ocurrido en el partido de Ensenada, Provincia de Buenos Aires.
Caso clínico
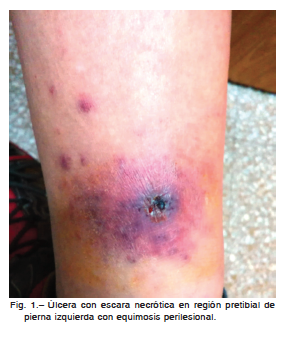
El paciente, de 40 años sin antecedentes de enfermedades, residente en Punta Lara, Ensenada, región suburbana próxima al Río de la Plata, consultó en febrero de 2016 por fiebre de 6 días de evolución y pápula eritematosa secundaria a mordedura de garrapata en región pretibial de pierna izquierda que evolucionó a úlcera con escara necrótica y equimosis perilesional (Fig. 1). Había recibido tratamiento en su lugar de residencia, sin mejoría, por lo que consultó en nuestro servicio. El cuadro febril comenzó 24 horas después de advertir la mordedura y presentó lesiones maculopapulares diseminadas en piel, astenia, cefalea, dolor retroocular y mioartralgias.
Ante la sospecha de fiebre manchada por rickettsias se solicitó: serología (par serológico), anatomía patológica de biopsia de piel, reacción en cadena de la polimerasa (PCR) en sangre y en biopsia de la lesión. Las muestras fueron enviadas al Instituto Nacional de Enfermedades Virales Humanas Dr. Julio Maiztegui. La investigación de IgG anti-antígenos de R. rickettsii mediante inmunofluorescencia indirecta resultó negativa en la primera muestra y positiva con título 1/128 en la segunda. Se inició tratamiento empírico con doxiciclina con evolución clínica favorable a las 72 h.
La conversión serológica confirmó la infección reciente por Rickettsia spp. La histopatología evidenció alteraciones asociadas a vasculitis necrotizante: infiltrado perivascular en dermis, presencia de linfocitos, macrófagos y escasos polimorfononucleares, asociados a focos de vasculitis de origen necrótico.
Se realizó la extracción del ADN de una muestra de sangre entera citratada y de una muestra de biopsia de la lesión de piel utilizando el kit DNAeasy Blood and Tissue kit (Qiagen, Alemania). Se realizó amplificación por PCR de un fragmento genómico correspondiente al gen gltA utilizando el set de oligonucleótidos CS78 y CS323 publicado previamente2; obteniéndose solo resultado positivo para la muestra de biopsia de piel. El producto de amplificación fue purificado y secuenciado utilizando un secuenciador ABI PRISM 3100 Avant Genetic Analyzer (Applied Biosystems, USA). La secuencia obtenida (343 nucléotidos) fue sometida a un análisis de comparación de secuencias con la herramienta BLAST para determinar similitudes con especies del género Rickettsias3. Luego, ésta fue alineada con otras secuencias de diferentes especies de Rickettsia disponibles en el GenBank utilizando la herramienta Clustal W contenida en el paquete BioEdit (versión 7.1.9)4. La secuencia del fragmento de 343 nt del gen gltA secuenciado de la muestra resultó 100% idéntica a la de cepas de R. parkeri previamente identificadas en Argentina y en diferentes países de América5, 6. Los números de acceso al GenBank para las cepas de R. parkeri utilizadas en el análisis fueron: EF102236, JN126320, KJ158742, KM245157, KF782319, KJ174527, KJ657733 Y U59732. El número de acceso al GenBank para la secuencia parcial del gen gltA de la cepa R. parkeri de Ensenada en este estudio es KY083055.
Además, se colectaron 4 garrapatas (3 hembras y 1 macho) sobre el perro del paciente. Las mismas fueron determinadas como Amblyomma triste en el Instituto Nacional de Tecnología Agropecuaria (INTA, Rafaela), y todas fueron negativas en el análisis molecular para la presencia de rickettsias tras la aplicación de la metodología de diagnóstico molecular descripta por Cicuttin y Nava7.
Discusión
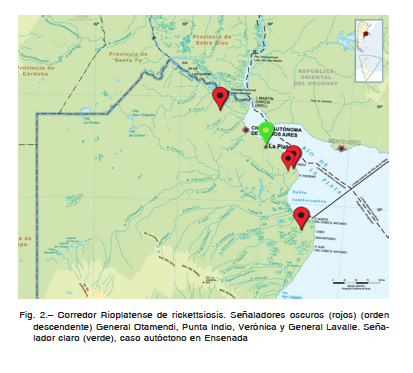
Las rickettsiosis transmitidas por garrapatas son causadas por bacterias intracelulares obligadas del género Rickettsia que pertenecen al grupo de las fiebres manchadas. La primera descripción de Rickettsia parkeri fue realizada por Parker et al. en 1939 en Amblyoma maculatum de cerdos pigmeos, en Texas, EE.UU.8. En 2004 se describió el primer caso clínico de la enfermedad en la costa Oeste de EE.UU.9. En Sudamérica, se comunicaron casos humanos en Uruguay y Argentina, donde R. parkeri fue hallada en las garrapatas A. triste y A. tigrinum (Argentina, Bolivia y Uruguay)1, 10. El primer caso en nuestro país fue diagnosticado en 2007 en el Delta del Paraná11, 12. En Buenos Aires además se informaron casos en General Lavalle, Verónica y Punta Indio, siendo el A. triste el vector atribuible13 (Fig. 2). Existen casos confirmados en San Luis, San Juan, Córdoba, La Rioja, Entre Ríos y La Pampa14.
Los adultos de Amblyomma triste se encuentran en mayor abundancia desde agosto a diciembre. Los adultos de Amblyomma tigrinum se hallan presentes durante todo el año, pero son más abundantes durante diciembre, enero y febrero. Estas características estacionales de los vectores aumentan las posibilidades de exposición a la enfermedad en esos meses del año, aumentando el riesgo de exposición en productores de ganado y personas que participan en actividades recreativas1, 13. La prevalencia de R. parkeri en A. triste en Argentina oscila entre el 7 y el 20%1.
R. parkeri provoca un cuadro clínico leve. Los síntomas y signos comienzan generalmente entre los 6 a 10 días posteriores de la mordedura por el artrópodo vector competente. En nuestro caso, el cuadro comenzó a las 24 h de advertida la mordedura con fiebre y lesión en piel. Es probable que el paciente no haya advertido la mordedura hasta que la garrapata aumentó considerablemente de tamaño, porque no es dolorosa y este ectoparásito es muy pequeño cuando inicia su alimentación. Los síntomas más frecuentes observados son fiebre (95-100%), malestar general, cefalea (75-83%), mialgias (75-92%), artralgias (cerca de 75%) y diferentes tipos de lesiones cutáneas (83% aproximadamente), que van desde un exantema maculo-papular o pápulo-vesicular leve a cuadros petequiales intensos, con presencia o no de escara de inoculación (92-95%) y linfadenopatía regional (25-30%)14, 15. El exantema puede comprometer manos y pies. Las manifestaciones clínicas y su evolución están estrechamente relacionadas con el mecanismo patogénico común a todas las rickettsiosis, que es la vasculitis de vasos pequeños y medianos. El principal signo clínico que distingue la infección por R. parkeri de la fiebre de las Montañas Rocosas por R. ricketsii es la frecuente presencia de una escara en el sitio de la mordedura de garrapata, similar a la “tache noir” de la fiebre exantemática mediterránea; además, su curso clínico benigno1, 10, 15, 16.
En los exámenes de laboratorio se puede encontrar trombocitopenia, leucopenia o leucocitosis, aumento de las enzimas hepáticas y de reactantes de fase aguda como la proteína C.
El diagnóstico se basa en la sospecha clínica, la amplificación del genoma bacteriano mediante técnicas moleculares y la detección de anticuerpos mediante técnicas serológicas como la inmunofluorescencia indirecta. Dado que la prevalencia de anticuerpos en la población sana puede ser elevada, un simple título de anticuerpos no debe ser considerado, por sí solo, diagnóstico de infección activa. Se debe obtener dos muestras de sueros, una en el periodo agudo (1ra muestra), previo al inicio de tratamiento con antibióticos y otro en la fase de convalecencia (tras dos semanas de iniciados los síntomas). En el caso aquí presentado, se confirmó el diagnóstico de rickettsiosis por conversión serológica10, 15.
Los métodos moleculares se han convertido en herramientas rápidas y específicas para la detección e identificación de rickettsias en distintas muestras (sangre, biopsias cutáneas, LCR, exudados, raspado de escaras y garrapatas). Requieren de secuenciación específica para determinar la especie del patógeno involucrada10, 15.
Se considera oportuno el tratamiento hasta el quinto día de fiebre y se debe iniciar ante la sospecha clínica sin esperar resultados confirmatorios. Para el grupo de las fiebres manchadas el tratamiento preferido es la doxiciclina (A-III) 100 mg cada 12 horas en adultos y 2.2 mg/kg cada 12 horas en niños < 45 kg, de 5 a 10 días de duración16. Se han descripto casos con evolución autolimitada, no existen hasta ahora informes sobre letalidad1, 10, 14, 15.
Agradecimientos: Se agradece al Instituto Anatomía Patológica (IAP) del INEVH, Pergamino, por los resultados de anatomía patológica obtenidos en el caso descripto.
Conflicto de intereses: Ninguno para declarar
Bibliografía
1. Angeletti V, Borras P, Yantorno L, et al. Guía de diagnóstico y tratamiento de la Fiebre Manchada por Rickettsia parkeri, 2016. CeNDIE ANLIS Dr. Carlos G. Malbran. Libro digital. ISBN. 978-987-24071-4-8. En:http://www.anlis.gov.ar/cendie/wp-content/uploads/2016/12/Manual-fiebre-manchada-2016-web.pdf; consultado octubre 2017.
2. Labruna MB, Whitworth T, Horta MC, et al. Rickettsia species infecting Amblyomma cooperi ticks from an area in the state of Sao Paulo, Brazil, where Brazilian spotted fever is endemic. J Clin Microbiol 2004: 42, 90-8.
3. Altschul SF, Gish W, Miller W, Myers EW, Lipman DJ. Basic local alignment search tool. J Mol Biol 1990; 215: 403-10.
4. Hall TA. BioEdit: a user-friendly biological sequence alignment editor and analysis program for Windows 95/98/NT. Nucl Acids Symp Ser 1999; 41: 95-8.
5. Monje LD, Nava S, Antoniazzi LR, Colombo VC, Beldomenico PM. In vitro isolation and infection intensity of Rickettsia parkeri in Amblyomma triste ticks from the Paraná River Delta region, Argentina. Ticks Tick Borne Dis 2014; 5: 924-7.
6. Melo AL, Alves AS, Nieri-Bastos FA, et al. Rickettsia parkeri infecting free-living Amblyomma triste ticks in the Brazilian Pantanal. Ticks Tick Borne Dis 2015; 6: 237-41.
7. Cicuttin G, Nava S. Molecular identification of Rickettsia parkeri infecting Amblyomma triste ticks in an area of Argentina where cases of rickettsiosis were diagnosed. Mem Inst Oswaldo Cruz 2013; 108: 123-5.
8. Parker RR, Kohls GM, Cox GW, et al. Observations on an infectious agent from Amblyomma maculatum. Public Health Reports 1939; 54: 1482-4.
9. Paddock CD, Sumner JW, Comer JA, et al. Rickettsia parkeri: A newly recognized cause of spotted fever rickettsiosis in the United States. Clin Infect Dis 2004; 38: 805-11.
10. Abarca K, Oteo JA. Aproximación clínica y principales rickettsiosis transmitidas por garrapatas presentes en Latinoamérica. Rev Chil Infectol 2014; 31: 569-76.
11. Seijo A, Picollo M, Nicholson W, Paddock C. Fiebre manchada por rickettsias en el Delta del Paraná: una enfermedad emergente. Medicina (B Aires) 2007; 67: 723-6.
12. Nava S, Elshenawy Y, Eremeeva M, Sumner JW, Mastropaolo M, Paddock CD. Rickettsia parkeri in Argentina. Emerg Infec Dis 2008; 14: 1894-7.
13. Romer Y, Nava S, Govedic F, et al. Rickettsia parkeri rickettsiosis in different ecological regions of Argentina and its association with Amblyomma tigrinum as a potential vector. Am J Trop Med Hyg 2014; 91: 1156-60.
14. Borras P, Carranza J, Lloveras S, et al. 2007-2017: 10 años de rickettsiosis por Rickettsia parkeri en Argentina. No publicado. 18th International Congress on Infectious Diseases. March 1-4, 2018. Final Abstract Number SADI 12.006.
15. Biggs HM, Behravesh CB, Bradley KK, et al. Diagnosis and management of tickborne rickettsial diseases: Rocky Mountain spotted fever and other spotted fever group rickettsioses, ehrlichioses, and anaplasmosis, United States. MMWR Recomm Rep 2016; 65 (No. RR-2): 1-44.
16. Saracho Bottero MN, Tarragona EL, Nava S. Spotted fever group rickettsiae in Amblyomma ticks likely to infest humans in rural areas from northwestern Argentina. Medicina (B Aires) 2015; 75: 391-5.
– – – –
All Faith is false, all Faith is true:
Truth is a shattered mirror strown
In myriad bits, while each one believes
His little bit the whole to own.
Todo credo es falso, todo credo es cierto.
Es la verdad un espejo que se ha roto
En mil añicos; pero cada cual se cree
Que poseer un fragmento es poseerlo todo.
Richard F. Burton (1821-1890)
The Kasidah of Haji Abdu El-Yezdi (1880). En: www.gutenberg.org; consultado el 6-6-2017. Traducción al castellano de Miguel Saénz. En: Day RA, Gastel B. Cómo escribir y publicar trabajos científicos. Washington DC: OPS/OMS, 2008. 4ta. Edición en español, p 82
