PABLO E. SARMIENTO, NICOLÁS ZADERENKO, ROBERTO M. A. COLQUE, FLORENCIA MELGAREJO OTAROLA, GUILLERMO PACHECO, FERNANDO J. DAGHERO, MIGUEL A. TIBALDI, EDUARDO MOREYRA (H)
Servicio de Cardiología, Sanatorio Allende, Sede Cerro, Córdoba, Argentina
Resumen La tromboembolia pulmonar aguda (TEPA) sigue siendo una importante causa de morbilidad y mortalidad a nivel mundial. Su diagnóstico, estratificación de riesgo y tratamiento precoz son fundamentales, siendo su pilar la anticoagulación. En pacientes de bajo riesgo cardiovascular, el pronóstico es excelente y solo basta con la administración de anticoagulantes. No obstante, debido al pobre pronóstico de los pacientes con riesgo elevado (descompensación hemodinámica), el enfoque terapéutico es más agresivo, utilizándose trombolíticos sistémicos que disminuyen la mortalidad pero incrementan el riesgo de complicaciones hemorrágicas mayores. En el TEPA de riesgo intermedio (evidencia de falla de ventrículo derecho, sin descompensación hemodinámica), la relación riesgo-beneficio del tratamiento con trombolíticos es más equilibrada por lo que la decisión es controvertida. La fragmentación mecánica con trombólisis dirigida por catéter es una alternativa con potenciales beneficios. Presentamos dos casos de TEPA de riesgo intermedio, en los que se realizó fragmentación mecánica y trombólisis dirigida por catéter.
Palabras clave: tromboembolia pulmonar aguda, riesgo intermedio, trombólisis dirigida por catéter
Abstract Acute pulmonary thromboembolism remains a significant cause of morbidity and mortality worldwide. Its diagnosis, risk stratification and early treatment are essential. The mainstay of treatment is anticoagulation. In patients with low cardiovascular risk, the prognosis is excellent and the treatment consists only of the administration of anticoagulants. Due to the poor prognosis of patients with high risk (hemodynamic decompensation), the approach is more aggressive using systemic thrombolytics, which reduce mortality but increase the risk of major hemorrhagic complications. In the intermediate-risk patients (evidence of right ventricular failure, without hemodynamic decompensation), the risk-benefit relationship of thrombolytic treatment is more balanced, so the choice is controversial. Mechanical fragmentation with catheter-directed thrombolysis is an alternative with potential benefits. We present two cases of intermediate-risk acute pulmonary thromboembolism to whom mechanical fragmentation and catheter-directed thrombolysis was applied.
Key words: acute pulmonary thromboembolism, intermediate risk catheter-directed thrombolysis
Dirección postal: Pablo E. Sarmiento, Sanatorio Allende, Laplace 5749 1er Piso, 5021 Córdoba, Argentina
e-mail: pabloesarmiento@gmail.com
El TEPA (tromboembolia pulmonar aguda) es la tercera causa de muerte en pacientes hospitalizados, con una incidencia estimada en 1/1000 1, 3. Aquellos que sobreviven pueden quedar con secuelas a largo plazo. Entre ellas; hipertensión pulmonar tromboembólica crónica, disfunción ventricular derecha persistente, intolerancia al ejercicio y reducida calidad de vida. Su presentación clínica es variable, pudiendo ocurrir en forma subclínica, sintomática con disnea súbita, dolor precordial o síncope y, en casos graves, con descompensación hemodinámica, shock cardiogénico o muerte súbita 4. Aquellos que presentan signos de falla de ventrículo derecho sin hipotensión son considerados como de riesgo intermedio y la decisión entre utilizar anticoagulantes asociados o no a trombolíticos, así como su vía de administración, es controvertida debido a las potenciales complicaciones 2. Se presentan dos casos de embolia de pulmón de riesgo intermedio tratados con fragmentación mecánica del trombo y trombolisis dirigida.
Caso clínico 1
Mujer de 62 años con antecedentes de cáncer de mama tratado quirúrgicamente y con radioterapia, en remisión desde 11 años atrás, y TEPA desde 3 años atrás, tratada con anticoagulantes orales por 1 año.
Consultó por guardia central refiriendo disnea súbita clase funcional (CF) III. Al ingreso, la frecuencia cardíaca era de 120 latidos por minuto; frecuencia respiratoria, 28 respiraciones por minuto; presión arterial, 100/60 mmHg; y saturación de O2 88% aire ambiente. En el resultado de los análisis se constató un dímero D de 6288 ng/ml, Nt-proBNP de 37 pg/ml y troponina T ultrasensible (TnTU) de 96 ng/l. El electrocardiograma (ECG) mostraba taquicardia sinusal y complejo de McGinn White (S1Q3T3), retardo de la conducción de la rama derecha y ondas T negativas de V1 a V4. En la radiografía de tórax se observó una sobreelevación del diafragma derecho.
La angiotomografía axial computarizada (angioTAC multislice de 64 cortes) de tórax reveló un TEPA central y periférico bilateral, de predominio derecho con alteración en la relación de ventrículo derecho (VD) y ventrículo izquierdo (VI). La paciente fue internada en la Unidad de Cuidados Coronarios (UCCo) y el ecocardiograma Doppler mostró dilatación del VD con desplazamiento del tabique interventricular. El score de Pulmonary Embolism Severity Index (PESI) fue de 152, por lo que se predijo un elevado riesgo de mortalidad a los 30 días.
Se interpretó el cuadro como TEPA de riesgo intermedio con signos de disfunción de VD por lo que se decidió la fragmentación mecánica del trombo y trombólisis local dirigida por catéter.
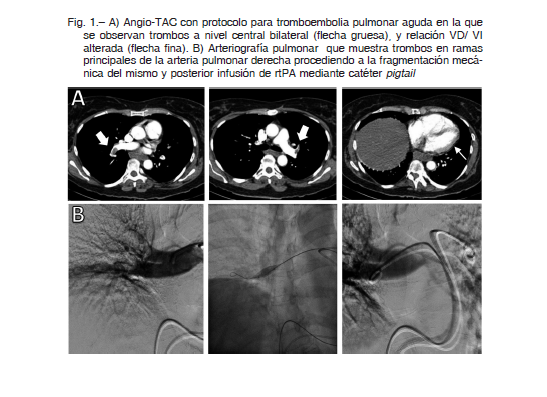
A través de un acceso venoso femoral derecho, se introdujo un catéter Judkin de coronaria derecha 6F, obteniendo los siguientes registros hemodinámicos: aurícula derecha, 10 mmHg; VD/0-20 mmHg; arteria pulmonar, 43/13 (28) mmHg; presión Wedge, 14 mmHg. Luego, se intercambiaron por un catéter tipo pigtail, se realizó una angiografía del árbol pulmonar en diferentes proyecciones, determinándose la presencia de trombos bilaterales localizados predominantes en las principales ramas del pulmón derecho. A causa de la abundante carga trombótica, se decidió realizar la fragmentación mecánica de los trombos con balón de 10 mm de diámetro, seguida de rotación del pigtail. Se obtuvo un acceso venoso femoral izquierdo y mediante dos catéteres pigtail en arterias pulmonar derecha e izquierda respectivamente, se realizó un bolo de 10 mg de tPA (alteplasa) (Fig. 1). Se inició infusión continua de 40 mg en 2 h y la administración de heparina de bajo peso molecular (HBPM), 1 mg/kg/12 h. Durante las siguientes 48 horas evolucionó favorablemente sin complicaciones de los accesos venosos y con mejoría clínica. Un control ecocardiográfico mostró normalización del tamaño del VD y una prueba de desafío con volumen señaló parámetros normales. Al sexto día de internación, se indicó el alta y tratamiento con rivaroxaban 15 mg cada 12 horas.
Caso clínico 2
Hombre de 61 años, ex tabaquista con antecedente de depresión y cáncer de colon avanzado diagnosticado 6 meses atrás, en tratamiento quimioterápico combinado.
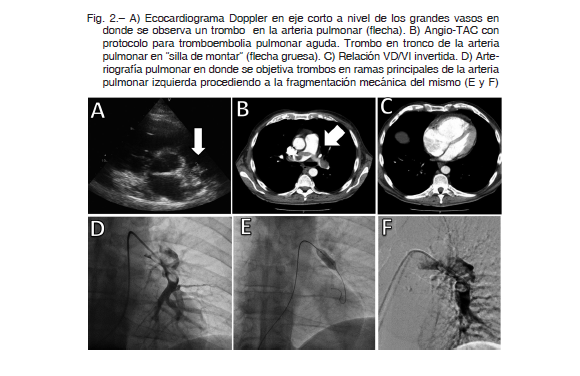
Consultó debido a astenia y síncopes recurrentes al ponerse de pie. Una angioTAC de tórax y abdomen objetivó un TEPA en “silla de montar” con dilatación del VD e inversión de la relación VD/VI por lo que se decidió internación en UCCo (Fig. 2).
El ECG mostró trastornos de la repolarización ventricular en cara anterior (T negativas). La radiografía de tórax no mostró anormalidades. El laboratorio reveló TnTU de 42.4 ng/l, Nt-proBNP de 4420 pg/ml y un dímero D de 19 985 ng/ml. Además, la gasometría arterial mostró alcalosis respiratoria.
El ecocardiograma Doppler reveló dilatación del tronco de la arteria pulmonar con evidencia de trombo a nivel de la bifurcación de la rama pulmonar derecha; dilatación considerable de cavidades derechas; insuficiencia tricúspidea grave e hipertensión pulmonar (PSAP estimada de 60 mmHg).
Se clasificó al TEPA como de riesgo intermedio resolviendo, junto con el servicio de oncología, la fragmentación mecánica del trombo con la administración de trombolíticos guiada por catéter, utilizando el protocolo descripto en el caso anterior seguido de tratamiento con enoxaparina (1 mg/kg/12 h).
Evolucionó favorablemente con pruebas de sedestación y bipedestación en las que no repitió síncope. En el ecocardiograma Doppler a las 72 horas se observó una disminución del tamaño de las cavidades derechas, manteniéndose las presiones pulmonares estimadas en 60 mmHg. La imagen de trombo en la arteria pulmonar había desaparecido. Una angioTAC de control demostró una disminución significativa del monto trombótico, permaneciendo aún trombos en ambas arterias pulmonares. Al quinto día de internación, se le dio el alta bajo tratamiento anticoagulante con HBPM
Discusión
El TEPA de riesgo intermedio cursa sin hipotensión arterial, pero con evidencia de compromiso del VD
reflejado por su disfunción o dilatación (relación VD/VI > 0.9), elevación de biomarcadores como ProBNP,
Nt-ProBNP, y troponinas T o I; o cambios electrocardiográficos consistentes en bloqueo completo de rama
derecha, trastornos de conducción de rama derecha o de la repolarización ventricular, o inversión de ondas T8. Con el objetivo de evitar sus complicaciones a largo plazo, la American Heart Association (AHA) y la European Heart Association (EHA) recomiendan el uso de trombolíticos sistémicos en pacientes seleccionados, mientras que el American College of Chest Physicians (ACCP) lo desaconseja y sugiere solo el uso de anticoagulantes 5-7 moderate-quality (Grade B. El rol de los trombolíticos administrados por vía sistémica versus anticoagulantes en pacientes de riesgo intermedio ha sido evaluado en numerosos estudios aleatorizados. El protocolo actualmente aprobado es la administración de 100 mg de tPA (alteplasa; Genentech, San Francisco, California) por vía endovenosa en un período de 2 horas 9. En conjunto, estos estudios mostraron que los trombolíticos mejoran la función del VD, reducen las presiones pulmonares y la tasa de descompensación hemodinámica a costa de un incremento del riesgo de complicaciones hemorrágicas mayores. Un meta análisis, en el cual el estudio PEITHO (The Pulmonary Embolism Thrombolysis Trial) contribuyó con más de la mitad de los pacientes, mostró una reducción de mortalidad del 52%, (OR 0.48, 95% CI 0.25-0.92) pero a costa de un incremento de la tasa de hemorragia intracerebral (1.46% vs. 0.19%, OR 4.63; 95 % CI 1.78-12.04). El riesgo de complicaciones hemorrágicas mayores fue 3 veces más elevado en pacientes mayores de 65 años 8,9.
Estos resultados llevaron a que se evaluara la hipótesis de que dosis más bajas de trombolíticos lograrían mantener los beneficios clínicos sin incrementar el riesgo de sangrado, lo cual fue demostrado en múltiples estudios aleatorizados y meta-análisis 10-12 2 hour recombinant tissue plasminogen activator (rt-PA.
Otra estrategia dirigida a reducir el riesgo hemorrágico es el tratamiento guiado por catéter. Este puede dividirse en trombólisis local guiada por catéter y en las técnicas mecánicas de disgregación del trombo, las cuales pueden realizarse mediante fragmentación con catéter, aspiración o trombo-fragmentación mediante ultrasonido. Estas técnicas promueven la remoción de trombo de las arterias pulmonares restituyendo el flujo sanguíneo a la circulación pulmonar y reduciendo la carga sobre el VD, lo que mejora el estado hemodinámico y la oxigenación. Las técnicas mecánicas de disgregación de trombo y trombólisis guiada por catéter pueden aplicarse por separado o concomitantemente, de acuerdo a la situación hemodinámica y al riesgo de sangrado del paciente. La administración local de fibrinolíticos permite dar dosis más bajas (tPA 10-24 mg) directamente en el interior del coagulo mediante el uso de catéteres con múltiples orificios laterales.
Las limitaciones de estas técnicas son el tamaño y la cronicidad de los trombos ya que, a medida que se van organizando, se van haciendo resistentes al tratamiento farmacológico y mecánico. No existen todavía estudios aleatorizados que hayan comparado la efectividad de las distintas técnicas mecánicas por catéter, aunque el registro PERFECT ha sugerido similar efectividad clínica y hemodinámica entre las distintas técnicas sin diferencias en la tasa de complicaciones. En cuanto a la comparación de las distintas técnicas guiadas por catéter con trombólisis sistémica, Aurora y colaboradores compararon ambas estrategias en 4426 pacientes de la Base de Datos Nacional de Readmisiones, entre 2013 y 2014. Encontraron que los pacientes tratados con trombólisis sistémica tuvieron mayor mortalidad (14.9% vs. 6.1%), combinación de mortalidad y sangrado mayor (18.1% vs. 8.4%) y tasa de readmisiones (10.6% vs. 7.6%). Liang y colaboradores evaluaron la Base de Datos Nacional de pacientes internados, encontrando similar mortalidad entre ambos grupos, pero menor tasa de sangrados intracerebrales. Esta evidencia sugiere que el abordaje guiado por catéter se asocia a menor riesgo de complicaciones hemorrágicas, con similar o mejor eficacia 13-15.
Los dos casos presentados, ingresaron hemodinámicamente estables, pero con evidencia de compromiso del VD, por lo que fueron clasificados en la categoría de riesgo intermedio. Se decidió realizar trombo fragmentación mecánica con trombólisis dirigida por catéter. Debido a que la dosis total de tPA administrada es cuatro veces menor a la dosis que debe administrarse en forma sistémica, se minimizó el riesgo de sangrado. Ambos casos mostraron disminución de la carga trombótica, mejoramiento de los parámetros clínicos y de la función del VD, sin que se produjeran complicaciones hemorrágicas.
Hasta que estudios aleatorizados establezcan cuál es la estrategia de tratamiento más apropiada para pacientes de riesgo intermedio, la decisión debería ser tomada por un equipo de cardiólogos y hemodinamistas en forma individualizada.
Conflicto de intereses: Ninguno para declarar
Bibliografía
1. Cáneva JO, Sheridan L, Klin P, Ossés JM, Valdivieso L, Wagner G. Trombólisis farmacológica y mecánica en tromboembolismo pulmonar y submasivo. Medicina (B Aires) 2014; 74: 124-6.
2. Dudzinski DM, Giri J, Rosenfield K. Interventional treatment of pulmonary embolism. Circ Cardiovasc Interv 2017; 10: pii: e004345.
3. Cohen AT, Agnelli G, Anderson FA, et al. Venous thromboembolism (VTE) in Europe. The number of VTE events and associated morbidity and mortality. Thromb Haemost 2007; 98: 756-64.
4. Miniati M, Prediletto R, Formichi B, et al. Accuracy of clinical assessment in the diagnosis of pulmonary embolism. Am J Respir Crit Care Med 1999; 159:864-71.
5. Konstantinides SV, Torbicki A, Agnelli G, et al. 2014 ESC guidelines on the diagnosis and management of acute pulmonary embolism. Eur Heart J 2014; 35: 3033-69.
6. Kearon C, Akl EA, Comerota AJ, et al. Antithrombotic therapy for VTE disease. Chest 2012;141: e419S-e496S.
7. Jaff MR, McMurtry MS, Archer SL, et al. Management of massive and submassive pulmonary embolism, iliofemoral deep vein thrombosis, and chronic thromboembolic pulmonary hypertension: A scientific statement from the american heart association. Circulation 2011; 123: 1788-30.
8. Bajaj A, Saleeb M, Rathor P, Sehgal V, Kabak B, Hosur S. Prognostic value of troponins in acute nonmassive pulmonary embolism: A meta-analysis. Hear Lung J Acute Crit Care 2015; 44: 327-34.
9. Konstantinides S, Geibel A, Heusel G, Heinrich F, Kasper W. Management Strategies and Prognosis of Pulmonary Embolism-3 Trial Investigators. Heparin plus alteplase compared with heparin alone in patients with submassive pulmonary embolism. N Engl J Med 2002; 347: 1143-50.
10. Sharifi M, Bay C, Skrocki L, Rahimi F, Mehdipour M, “MOPETT” Investigators. Moderate pulmonary embolism treated with thrombolysis (from the MOPETT Trial). Am J Cardiol 2013; 111: 273-7.
11. Wang C, Zhai Z, Yang Y, et al. Efficacy and safety of low dose recombinant tissue-type plasminogen activator for the treatment of acute pulmonary thromboembolism: a randomized, multicenter, controlled trial. Chest 2010; 137: 254-62.
12. Zhang Z, Zhai Z, Liang L, Liu F, Yang Y, Wang C. Lower dosage of recombinant tissue-type plasminogen activator (rt-PA) in the treatment of acute pulmonary embolism: a systematic review and meta-analysis. Thromb Res 2014; 133: 357-63.
13. Mohan B, Aslam N, Kumar Mehra A, et al. Impact of catheter fragmentation followed by local intrapulmonary thrombolysis in acute high risk pulmonary embolism as primary therapy. Indian Heart J 2014; 66:294-301.
14. Piazza G, Hohlfelder B, Jaff MR, et al. A prospective, single-arm, multicentertTrial of ultrasound-facilitated, catheter-directed, low-dose fibrinolysis for acute massive and submassive pulmonarye embolism: The SEATTLE II Study. JACC Cardiovasc Interv 2015; 8:1382-92.
15. Kuo WT, Banerjee A, Kim PS, et al. Pulmonary Embolism Response to Fragmentation, Embolectomy, and Catheter Thrombolysis (PERFECT): Initial results from a prospective multicenter registry. Chest 2015; 148: 667-73.
