LUCIANA E. GIONO
Departamento de Fisiología, Biología Molecular y Celular, Facultad de Ciencias Exactas y Naturales, Universidad de Buenos Aires, Instituto de Fisiología, Biología Molecular y Neurociencias (IFIBYNE), CONICET-Universidad de Buenos Aires, Buenos Aires, Argentina
Resumen El desarrollo de técnicas que permitan editar o corregir con precisión y eficiencia el genoma de
células vivas es uno de los objetivos principales de la investigación biomédica. En las últimas décadas se han investigado e implementado distintas herramientas de edición genómica entre las cuales se destaca el sistema CRISPR/Cas9, un mecanismo de defensa bacteriano que ha sido adaptado y rediseñado para su utilización en otros modelos celulares. La accesibilidad, técnica y económica, y el enorme potencial de CRISPR/Cas9 han dado lugar a una revolución casi sin precedentes en las ciencias biomédicas y representan un gran avance en el campo de la terapia génica que requiere, sin embargo, la cautela apropiada.
Palabras clave: CRISPR/Cas9, edición genómica, terapia génica, embriones humanos
Abstract CRISPR/Cas9 and gene therapy. The development of techniques that allow the precise and efficient
edition of the genome of living cells is one of the main goals of biomedical research. Over the last few decades, a number of genome editing tools have been developed, the most prominent being the CRISPR/Cas9 system, a bacterial defense mechanism that has been redesigned for its use in other cellular systems. The accessibility, both technical and economical, and the enormous potential of CRISPR/Cas9 have contributed to an almost unprecedented revolution in the biomedical sciences and represent an important step forward in the field of gene therapy that needs, however, to be taken cautiously.
Key words: CRISPR/Cas9, genome editing, gene therapy, human embryos
Recibido: 29-VIII-2017 Aceptado: 4-IX-2017
Dirección postal: Luciana E. Giono, Facultad de Ciencias Exactas y Naturales, UBA, Ciudad Universitaria, Pabellón II, 1428 Buenos Aires, Argentina
e-mail: lgiono@fbmc.fcen.uba.ar
Se conocen más de 10 000 enfermedades hereditarias monogénicas (causadas por un único gen) que afectan a millones de personas en todo el mundo. Algunas de estas enfermedades son causadas por mutaciones autosómicas dominantes, es decir que la herencia de una única copia defectuosa del gen responsable puede causar síntomas clínicos1. El desarrollo de técnicas que permitan editar o corregir con precisión y eficiencia el genoma de células vivas es, por lo tanto, uno de los objetivos principales de la investigación biomédica.
Hace unas semanas, CRISPR/Cas9 fue tapa de diarios y revistas en todo el mundo a raíz de un trabajo realizado por un equipo internacional de investigadores de la Universidad de Oregón, en EE.UU. y publicado en la revista Nature. En este artículo, se describió el uso de la técnica de edición génica CRISPR/Cas9 para corregir una mutación patogénica en docenas de embriones humanos viables1.
El concepto de la edición genómica
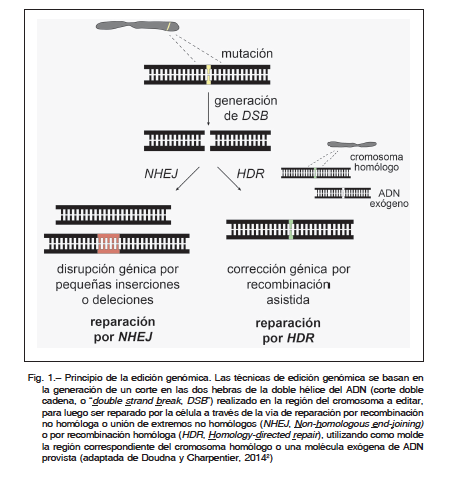
Las metodologías de edición genómica desarrolladas hasta el momento se basan en la generación de un corte en las dos hebras de la doble hélice del ADN (llamado corte doble cadena, o double strand break, DSB) realizado en forma precisa y dirigida en la región a editar. Este corte es luego reparado por la célula que dispone, para esto, de dos mecanismos alternativos. La vía de reparación preferencial es la recombinación no homóloga o unión de extremos no homólogos (cuya sigla en inglés es NHEJ por Non-homologous end-joining). Este mecanismo consiste en la simple unión de los extremos generados y típicamente introduce mutaciones adicionales al generar inserciones o deleciones en la zona de la unión. La otra vía de reparación es la recombinación homóloga (cuya sigla en inglés es HR o HDR por Homologous recombination o Homology-directed repair) que puede utilizar como molde la región correspondiente del cromosoma homólogo o una molécula exógena de ADN provista para llevar a cabo la correcta unión de los extremos (Fig. 1)2. El cromosoma así editado es luego heredado por las células hijas.
Las técnicas de edición genómica para aplicaciones clínicas se enfrentan entonces a tres desafíos principales:
1) Generar el DSB en forma eficiente y precisa, es decir en la secuencia que contiene la mutación o en la zona que se desea editar, y únicamente allí. Este desafío plantea uno adicional, que es el desarrollo de técnicas extremadamente sensibles para detectar si se generaron cortes no deseados (off-target) en otras regiones del genoma.
2) Conseguir una reparación correcta del DSB. Esto implica vencer la baja eficiencia de la vía HDR frente a la vía NHEJ y/o monitorear y seleccionar aquellas células en las que la reparación fue efectuada correctamente (la reparación por la vía NHEJ es frecuentemente utilizada en la investigación cuando se busca interrumpir un gen para estudiar su función, pero es inaceptable en las aplicaciones clínicas, a menos que el objetivo sea precisamente anular la función de un gen).
3) En el caso de la edición genómica para la obtención de embriones, lograr llevar a cabo la edición en un punto del desarrollo lo suficientemente temprano, de forma que todas las células del organismo posean la secuencia editada y no se generen organismos “mosaico”, donde algunas células porten la versión corregida pero otras conserven la versión original, mutada. Además del problema obvio de que algunas células mantendrían la mutación, la generación de organismos mosaico dificultaría considerablemente el diagnóstico genético preimplantatorio.
En las últimas décadas se han investigado y desarrollado distintas metodologías con el objetivo de superar estos desafíos, principalmente el primero: la capacidad de dirigir una nucleasa (las enzimas que cortan ácidos nucleicos) a una secuencia determinada del ADN, a elección del investigador. Esto representa, en otras palabras, la capacidad de diseñar una proteína, u otro tipo de molécula, capaz de encontrar eficientemente una aguja en un pajar. Entre ellas se encuentran las meganucleasas, las nucleasas efectoras tipo activador de transcripción (Transcription Activator-Like Effector Nucleases o TALENs) y las nucleasas con dominios de dedos de zinc (Zinc Finger Nucleases o ZFNs), actualmente testeadas en ensayos clínicos. Por supuesto, cada uno de estos métodos tiene sus limitaciones, incluyendo los efectos
off-target, restricciones en cuanto a las secuencias que pueden ser reconocidas y el costo y la complejidad para desarrollar estas enzimas3, 4. Y entonces surgió CRISPR/Cas9.
La revolución CRISPR/Cas9
Nuestro conocimiento del sistema conocido actualmente como CRISPR/Cas9 y su aprovechamiento como herramienta de ingeniería genética es el fruto de un rompecabezas construido, a lo largo de más de dos décadas, por microbiólogos de todo el mundo5. Se han descripto, en diversas especies de microorganismos, varios tipos de sistemas CRISPR de variado grado de complejidad que permiten a sus portadores defenderse de virus y otros ADNs foráneos. Los componentes de este sistema son utilizados por los microorganismos para generar una especie de “catálogo” de los ADN virales con los que se encuentran. Al producirse un segundo encuentro con el virus, los microorganismos realizan una copia de estas secuencias almacenadas (denominada “ARN guía”) para reconocer a las moléculas de ADN invasor, dirigir a la nucleasa Cas9 y cortarlas para luego eliminarlas. Se trata, así, de un sistema inmune adaptativo.
El estudio detallado de estos mecanismos permitió plantear la posibilidad de utilizarlo en otros sistemas celulares para guiar a la nucleasa Cas9 en forma específica hacia otras secuencias. Esto requirió una extensa labor de optimización para conseguir, por ejemplo, que la nucleasa bacteriana se dirija al núcleo de las células eucariotas6. Este trabajo se convirtió en el artículo más citado del campo y generó un conjunto de reactivos que recibió, en los 3 años siguientes, más de 25 mil pedidos por parte de otros laboratorios del mundo5.
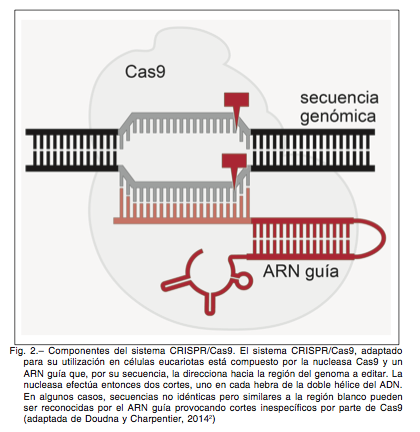
La secuencia blanco que es cortada por Cas9 está determinada por la secuencia del ARN guía, por lo que basta con sintetizar una nueva molécula de ARN para redireccionar a la nucleasa hacia otro gen (Fig. 2). En este aspecto, CRISPR se distingue de las nucleasas mencionadas anteriormente para las que, por cada secuencia que se quiere editar, se requiere diseñar una nueva enzima. Esto convierte al sistema CRISPR/Cas9 en una técnica de edición genómica extremadamente simple y accesible (económica y técnicamente) comparada con los métodos disponibles hasta su descubrimiento.
Rápidamente, CRISPR fue adaptado y rediseñado para un amplio abanico de aplicaciones: el encendido o apagado de genes específicos para el estudio de su función, el desarrollo de estudios en gran escala (con una gran población de ARN guías distintos) para la identificación de genes involucrados en un proceso celular determinado, la creación de modelos animales de enfermedades humanas, el direccionamiento de proteínas a secuencias específicas del genoma y la modificación genética de plantas, entre muchas otras2.
La edición genómica de embriones por CRISPR/Cas9
En los últimos años hubieron varios intentos de corrección de células y/o embriones humanos utilizando la técnica de CRISPR/Cas9, en algunos de los cuales se observó una alta tasa de efectos off-target y de mosaicismo7. Esto pone en evidencia la necesidad, por un lado, de una mayor comprensión del funcionamiento del sistema CRISPR así como del entorno celular en el que opera la nucleasa y, por el otro, de una extremada cautela en su utilización.
En el reciente trabajo publicado en la revista Nature, un grupo de investigadores dirigido por el especialista en biología reproductiva Shoukhrat Mitalipov eligió una mutación en el gen MYBPC3 que causa miocardiopatía hipertrófica, una enfermedad hereditaria que afecta aproximadamente a 1 de cada 500 personas1. En el trabajo, esperma donado por un hombre portador de una mutación dominante (una deleción de 4 nucleótidos) fue utilizado para fertilizar in vitro oocitos normales. Dado que el donante era un heterocigota portador de la mutación, un 50% de sus espermatozoides llevarían la copia normal, salvaje, del gen MYBPC3 mientras que el otro 50% llevaría la copia mutada, generando, en ausencia de todo tratamiento, un 50% de embriones normales y un 50% de embriones portadores de la mutación.
El trabajo se destacó, con respecto a intentos anteriores, por su alta eficiencia de edición, reflejada tanto en una alta tasa de corrección de la mutación como en una baja generación de embriones mosaico. La estrategia de los investigadores consistió, en primer lugar, en inyectar los componentes del sistema CRISPR/Cas9 junto con el esperma, en oocitos arrestados en metafase II (inyección intracitoplasmática de esperma). Esto aumentaría la probabilidad de que la nucleasa Cas9 actúe antes de la primera duplicación del alelo paterno mutado. En segundo lugar, se eligió inyectar directamente la proteína recombinante junto con la molécula ARN guía en vez de introducir la secuencia de ADN que codifica la proteína Cas9 para permitir que ésta se fabrique en las células. De esta manera, la proteína Cas9 se encontraría activa en las células durante un período de tiempo acotado, hasta degradarse, reduciendo la exposición a la actividad de la nucleasa y, por lo tanto, la probabilidad de que se sigan generado cortes (específicos o inespecíficos) en el genoma del cigoto.
En estas condiciones, se obtuvo un 72% de embriones correctamente editados, es decir un 22% de reparación precisa (vía HDR) y de aumento de embriones normales con respecto al 50% esperado. En el 28% de los embriones analizados, los cortes generados por Cas9 habían sido reparados por la vía NHEJ generando inserciones y deleciones en el gen MYBPC3 y éstos habrían sido, por lo tanto, descartados. Un estudio exhaustivo, si bien no completo, no detectó ningún corte inespecífico no deseado por parte de la nucleasa Cas91.
Perspectivas para el futuro
La revolución desencadenada por el sistema CRISPR/Cas9 casi no tiene precedentes en las ciencias biológicas. Su simpleza y economía lo pone al alcance de todos y su potencial es, en principio, inmenso. Desde la terapia génica hasta la modificación de especies vegetales, pasando por su introducción en la naturaleza para la erradicación de especies de mosquitos portadores de parásitos, el desarrollo de CRISPR/Cas9 ha generado tanto entusiasmo como alarma y, como siempre, los organismos regulatorios pertinentes deberán ponerse al día con la tecnología8, 9.
En el terreno de la clínica, la técnica se enfrenta todavía a ciertas limitaciones. A los desafíos ya mencionados (la eficiencia y precisión de los cortes generados por Cas9, la eliminación y/o reducción de cortes off-target y su detección, la reparación correcta de los cortes por la vía HDR, la obtención de mosaicos) se suma el de la vía de administración de los componentes del sistema: la nucleasa Cas9 y el ARN guía.
En un escenario de fecundación in vitro y diagnóstico preimplantatorio como el del trabajo de Mitalipov, ¿qué sentido tendría la edición genómica por CRISPR, siendo que la mitad de los embriones ya eran de por sí normales? De hecho, el trabajo constituyó simplemente una prueba de principio y los embriones obtenidos no fueron implantados.
Es razonable esperar que los primeros ensayos que utilicen la técnica de CRISPR/Cas9 correspondan a situaciones en las que los componentes de CRISPR puedan ser inyectados o administrados directamente en los tejidos blanco o en los que las células afectadas puedan ser recolectadas del cuerpo, editadas y luego reintroducidas8. De hecho, el sitio clinicaltrials.gov de EE.UU. registra, al día de la fecha, nueve ensayos clínicos que utilizan la tecnología CRISPR/Cas9 para la edición de genes, ocho de los cuales están basados en la modificación de células del sistema inmune-hematopoyético y uno en el tratamiento de la neoplasia cervical asociada a HPV.
La posibilidad que hoy existe de utilizar el sistema CRISPR/Cas9 para la edición genómica y sus múltiples aplicaciones, es el resultado de un esfuerzo colectivo que comienza en 1995 con la curiosidad suscitada por unas secuencias repetidas de función desconocida, encontradas en un microorganismo en la costa de Alicante en España10, y culmina en 2012 con la reconstrucción en un tubo de ensayo del sistema CRISPR/Cas9 purificado en dos laboratorios independientes en EE.UU.11, 12. Ninguno de estos investigadores estudiaba enfermedades humanas, ni pretendía encontrar una técnica que permitiera corregirlas. La historia del descubrimiento de CRISPR/Cas9 y la revolución que representa para las ciencias biomédicas ilustran el espectacular salto que, de manera imprevista, puede darse entre la ciencia “básica” y la ciencia “aplicada” y el error en que se incurre al hacer esta distinción.
Conflicto de intereses: Ninguno para declarar
Bibliografía
1. Ma H, Marti-Gutierrez N, Park SW, et al. Correction of a pathogenic gene mutation in human embryos. Nature 2017; 548: 413-9.
2. Doudna JA, Charpentier E. Genome editing. The new frontier of genome engineering with CRISPR-Cas9. Science 2014; 346: 1258096.
3. Brookhouser N, Raman S, Potts C, Brafman DA. May I cut in? Gene editing approaches in human induced pluripotent stem cells. Cells 2017; 6. pii: E5. doi: 10.3390/cells6010005.
4. Gaj T, Gersbach CA, Barbas CF, 3rd. ZFN, TALEN, and CRISPR/Cas-based methods for genome engineering. Trends Biotechnol 2013; 31: 397-405.
5. Lander ES. The Heroes of CRISPR. Cell 2016; 164:18-28.
6. Cong L, Ran FA, Cox D, et al. Multiplex genome engineering using CRISPR/Cas systems. Science 2013; 339: 819-23.
7. Liang P, Xu Y, Zhang X, et al. CRISPR/Cas9-mediated gene editing in human tripronuclear zygotes. Protein Cell 2015; 6: 363-72.
8. Ledford H. CRISPR, the disruptor. Nature 2015; 522:20-4.
9. Baltimore D, Berg P, Botchan M, et al. Biotechnology. A prudent path forward for genomic engineering and germline gene modification. Science 2015; 348: 36-8.
10. Mojica FJ, Ferrer C, Juez G, Rodríguez-Valera F. Long stretches of short tandem repeats are present in the largest replicons of the Archaea Haloferax mediterranei and Haloferax volcanii and could be involved in replicon partitioning. Mol Microbiol 1995; 17:85-93.
11. Gasiunas G, Barrangou R, Horvath P, Siksnys V. Cas9-crRNA ribonucleoprotein complex mediates specific DNA cleavage for adaptive immunity in bacteria. Proc Natl Acad Sci U S A 2012; 109: E2579-86.
12. Jinek M, Chylinski K, Fonfara I, Hauer M, Doudna JA, Charpentier E. A programmable dual-RNA-guided DNA endonuclease in adaptive bacterial immunity. Science 2012; 337: 816-21.
– – – –
Las vicisitudes de mi vida y el ardiente deseo de instruirme en muy diferentes materias, me obligaron a ocuparme durante muchos años, y exclusivamente en apariencia, en el estudio de ciencias especiales, como la botánica, la geología, la química, la astronomía y el magnetismo terrestre. Preparación necesaria era esta, si habían de emprenderse con utilidad lejanos viajes; pero también tales trabajos tenían otro objeto más elevado: el de comprender el mundo de los fenómenos y de las formas físicas en su conexión y mutua influencia. Desde mi primera edad he tenido la suerte de escuchar los benévolos consejos de hombres superiores, convenciéndome desde luego de que si no se poseen sólidos conocimientos relativos a las diversas partes de las ciencias naturales, la contemplación de la naturaleza en más extensos horizontes, como el intento de comprender las leyes porque se rige la física del mundo, sería solo vana y quimérica empresa.
Alejandro de Humboldt (1769-1859)
Cosmos. Ensayo de una descripción física del mundo. Vertido al castellano para la Biblioteca Hispano-Sur-Americana. Bélgica: Eduardo Perié, 1875. Tomo I. Prefacio IV. Con leves modificaciones ortográficas.
