MARÍA DEL CARMEN SAAVEDRA, LAURA M. RIERA, ALEJANDRO J. BOTTALE, MAURICIO A. MARIANI, ANDREA S. MAIZA, ANA MARÍA AMBROSIO
Instituto Nacional de Enfermedades Virales Humanas Dr. Julio I. Maiztegui (INEVH-ANLIS), Pergamino, Buenos Aires, Argentina
Resumen Candid#1 es la primera vacuna a virus vivo atenuado producida y registrada en Argentina. Se produce en el INEVH desde 2003 para prevenir la fiebre hemorrágica argentina y se obtiene mediante cosecha de sobrenadantes de cultivos de células diploides infectadas con una cepa atenuada del virus Junín, formulación y posterior liofilización. Su estabilidad es crucial para asegurar su efectividad. El objetivo de este trabajo fue evaluar la estabilidad de Candid#1 exponiéndola a distintas condiciones de temperatura y tiempo. Tres lotes producidos en 2003 fueron sometidos al siguiente esquema de almacenamiento: (a) vacuna reconsti- tuida conservada entre 2 °C y 8 °C durante 8 días, (b) vacuna liofilizada conservada entre 2 °C y 8 °C durante 6 meses, y (c) vacuna liofilizada conservada entre -18 °C y -20 °C durante 10 años. La potencia fue evaluada en monocapa de células Vero bajo agar. Los resultados fueron: (a) Candid#1 reconstituida fue estable 8 días entre 2 °C y 8 °C, (b) Candid#1 liofilizada fue estable 2 meses entre 2 °C y 8 °C y (c) Candid#1 liofilizada fue estable 9 años entre -18 °C y -20 °C manteniendo todos sus atributos. Estos resultados permitieron establecer las siguientes condiciones de almacenamiento: reconstituida 12 horas entre 2 °C y 8 °C, liofilizada 30 días entre 2 °C y 8 °C y 9 años entre -18 °C y -20 °C. A la luz de estos resultados, se generaron cambios favorables en las condiciones de transporte, almacenamiento y distribución de la vacuna. Se implementó la instalación de freezers domésticos en centros estratégicamente distribuidos, permitiendo preservar stocks de vacuna y distribuir las dosis necesarias a vacunatorios.
Palabras clave: virus Junín, potencia de vacuna, almacenamiento de vacunas
Abstract Stability of Candid#1 vaccine to prevent Argentine Hemorrhagic Fever. Candid#1 is the first live attenuated vaccine produced and registered in Argentina. Produced since 2003 at the INEVH to prevent Argentine hemorrhagic fever, it is obtained by harvesting supernatants of diploid cells infected with an attenuated strain of Junin virus and subsequent lyophilization. The stability of this vaccine is crucial to ensure its effectiveness. This study was aimed to evaluate the stability of Candid#1 by exposing it to different time and temperature conditions. Three vaccine batches produced in 2003 were analysed according to the following stor- age scheme: (a) reconstituted vaccine at 2 °C to 8°C for 8 days; (b) lyophilized vaccine at 2 °C to 8 °C for 6 months; (c) lyophilized vaccine at -18 °C to -20 °C for 10 years. The potency was assessed in Vero cell mono- layers under agar. The results were: (a) reconstituted vaccine was stable between 2 °C and 8 °C for 8 days, (b) lyophilized vaccine was stable between 2 °C and 8 °C for 2 months, and (c) lyophilized vaccine was stable 9 years between -18 °C and -20 °C, keeping all its properties. These results allowed us to establish the following storage conditions and expiration times for Candid#1: (a) reconstituted: 12 hours between 2 °C and 8 °C, (b) lyophilized: 30 days between 2 °C and 8 °C and (c) lyophilized: 9 years between -18 °C and -20 °C. Based on our results, favorable changes were made in the conditions of transport, storage and distribution of the vaccine. Domestic freezers in strategically located centers were installed, allowing the preservation of vaccine stocks for distribution to secondary vaccination centers.
Key words: Junin virus, vaccine potency, vaccine storage
Recibido: 23-V-2017 Aceptado: 26-VII-2017
Dirección postal: Dra. María del Carmen Saavedra, Instituto Nacional de Enfermedades Virales Humanas Dr. Julio I. Maiztegui, Monteagudo 2510, 2700 Pergamino, Buenos Aires, Argentina
e-mail: carmensaavedra_ar@yahoo.com.ar
La fiebre hemorrágica argentina es una enfermedad aguda producida por el virus Junín1, 2 para cuya prevención existe una vacuna a virus Junín vivo atenuado. La cepa atenuada Candid#13 ha dado su denominación a la vacuna. Esta vacuna es considerada una droga “huérfana”4 ya que está destinada a una enfermedad de muy baja prevalencia y de circulación restringida a un área geográfica reducida, por lo que su comercialización no recupera los costos de desarrollo, producción y distribución. Este tipo de producto, por consiguiente, no es de interés para la industria farmacéutica y generalmente su producción es asumida por ONGs o por los gobiernos de cada país. Esta condición fue anticipada desde el desarrollo de Candid#1, por lo que fue previsto que, en Argentina, el productor de esta vacuna fuera el Instituto Nacional de Enfermedades Virales Humanas Dr. Julio I. Maiztegui (INEVH-ANLIS)5-7, dependiente del Ministerio de Salud de la Nación.
Candid#1 se obtiene por cosecha de sobrenadantes de cultivos de células diploides infectados con la semilla vacunal3. Estos sobrenadantes son formulados y dosificados para ser sometidos a un proceso de liofilización. Luego de la realización del ensayo clínico puente diseñado para comparar la vacuna Candid#1 producida en Argentina con la producida en EE.UU. se obtuvo el registro de la misma por la Autoridad Regulatoria Nacional (Resolución de ANMAT N ° 4882, Agosto 2006), y en 2007 fue incorporada al Calendario Nacional de Inmunizaciones8, 9.
La utilización de las vacunas implica su llegada a la población blanco en las mismas condiciones en que se ha determinado su capacidad inmunizante. Para ello se deben desarrollar estrategias de distribución y almacenamiento de las vacunas basadas en sus condiciones de estabilidad10, 11. La estabilidad de un producto farmacéutico se define como la capacidad para conservar sus propiedades químicas, físicas, microbiológicas y biofarmacéuticas a lo largo de su tiempo de conservación dentro de límites especificados.
Existen dos tipos de factores que afectan la estabilidad de las vacunas: (i) los factores intrínsecos que están relacionados con los procesos de su fabricación y los componentes de la vacuna; y (ii) los factores externos o extrínsecos, donde se puede intervenir minimizando o eliminado aquellos que pueden afectar la estabilidad.
La temperatura es sin duda el factor que más puede afectar la estabilidad. Cuando la vacuna es expuesta a temperaturas por encima o por debajo de lo recomendado se produce pérdida de su potencia. El daño que ocasione la temperatura estará en relación directa al tiempo de exposición y a las características de la vacuna (liofilizada o reconstituida). En virtud de lo expuesto y de la natural termolabilidad de los arenavirus, y particularmente del virus Junín, se diseñó un programa de ensayos para determinar las condiciones de temperatura en que se debe conservar esta vacuna a fin de preservar sus atributos originales. Este programa fue parte del protocolo de desarrollo de Candid#1 y respondió a requerimientos de la autoridad regulatoria argentina12.
Presentamos aquí los resultados de los ensayos con Candid#1 liofilizada y reconstituida realizados en tiempo real entre 2004 y 2014 para definir las condiciones adecuadas de almacenamiento y distribución y establecer su período de vida útil.
Materiales y métodos
Fueron empleados el Lote A1, el Lote A2 y el Lote A3 de la Vacuna Candid#1 (XJ Cob2 Cer R44 FRhL– 219) producida en INEVH-ANLIS (REM N° 53205, Disposición ANMAT N° 4882). Cada frasco de vacuna fue reconstituido en 5.5 ml de diluente, equivalente a 10 dosis de vacuna por frasco. El diluente de la vacuna (ampollas de agua estéril para inyección) fue producido en el INEVH-ANLIS (REM N° 51663, Disposición ANMAT N° 5399).
Las células Vero (ATCC-CCL81), células epiteliales de riñón de mono verde africano (Cercopithecus aethiops) certificadas, se utilizaron para la prueba de potencia entre los pasajes 32 y 42.
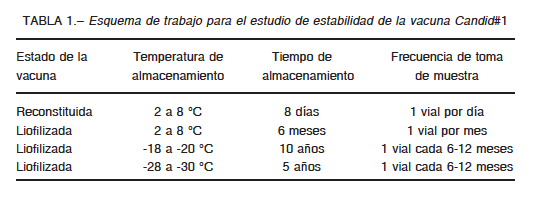
El esquema de trabajo fue: Los lotes A1, A2 y A3 de vacuna Candid#1 liofilizada fueron inicialmente almacenados entre -28 °C y -30 °C. Desde estas condiciones de temperatura fueron muestreados entre 39 y 41 viales de cada lote para el estudio a diferentes temperaturas de almacenamiento como se esquematiza en la Tabla 1:
a) Vacuna reconstituida. Se reconstituyeron 8 viales de vacuna de cada lote y, antes de ser guardados en la heladera (2 °C a 8 °C), se observó el aspecto de cada uno de ellos. Se retiró de la heladera un frasco por día durante 8 días, que se guardó a -70 °C para la posterior determinación de potencia.
b) Vacuna liofilizada, temperatura de almacenamiento 2 °C a 8 °C. Se guardaron en la heladera 6 viales de vacuna liofilizada de cada lote y se retiró un frasco por mes durante 6 meses, luego fueron almacenados a -70 °C para la posterior determinación de potencia.
c) Vacuna liofilizada, temperatura de almacenamiento -18 °C a -20 °C. Se guardó a dicha temperatura una cantidad suficiente de viales de vacuna liofilizada y se retiró un vial de vacuna de cada lote cada 6-12 meses durante 10 años, entre -18 °C y -20 °C para determinación de potencia, humedad residual, pH y osmolaridad.
d) Vacuna liofilizada, temperatura de almacenamiento -28 a -30 °C. Se controló un vial de vacuna de cada lote cada 6-12 meses durante 5 años a la temperatura original de almacenamiento para determinación de potencia, humedad residual, pH y osmolaridad.
Para el ensayo de potencia13 se realizó la titulación de la vacuna Candid#1 mediante la inoculación de diferentes diluciones de la misma en células Vero, y posterior agregado de una cubierta de agarosa y colorante supravital, lo que permitió
visualizar las áreas focales de infección (placas) y realizar su conteo. Se utilizó como testigo una cepa de referencia interna Candid#1. La prueba se consideró válida al evaluar el título del virus de referencia y compararla con la Carta Control. Se utilizó como guía las reglas de Westgard14 sobre Cartas de Control de Shewart15. La especificación de potencia para la vacuna Candid#1 es entre 1.00 × 104 y 9.00 × 105 UFP/ml.
La osmolaridad fue determinada mediante el método de depresión en el punto de congelamiento16. Se utilizó el osmómetro Advanced Modelo 3250, con certificado de calibración vigente (especificación: 260-330 mOsm/kg).
La humedad residual fue determinada mediante el método Karl Fisher17. Se utilizó el titulador Mettler Toledo DL31, con certificado de calibración vigente. La técnica consiste en someter un electrodo de platino a una corriente eléctrica constante. El iodo adicionado reacciona con el agua presente en la muestra. El punto final es el iodo libre en la solución, ese iodo libre transporta electrones, solución conductora. Para mantener la corriente constante la tensión se reduce. La reducción del valor de la tensión a un cierto valor es la indicación del punto final de la valoración. Especificación: < 3%.
El pH fue determinado mediante el método potencio-métrico18. Se utilizó un peachímetro calibrado, con especificación pH 6.5-7.5.
Las temperaturas -18 °C a -20 °C y -28 °C a -30 °C fueron supervisadas en las respectivas cámaras de modo continuo mediante el sistema SCADA (Supervisory, Control and Data Adquisition) (Excel Building Supervisor, Versión 1.4.3. Marca Honeywell).
Resultados
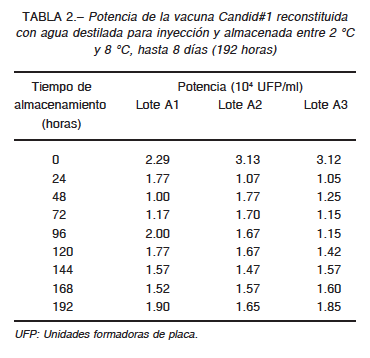
No se detectó ningún parámetro anormal en el aspecto (turbidez, color, partículas) de cada uno de los viales reconstituidos de vacuna conservada entre 2 °C y 8 °C. Con respecto al ensayo de potencia, la vacuna Candid#1 reconstituida resultó estable entre 2 °C y 8 °C durante 8 días manteniendo un título de virus entre 1.00 × 104 y 3.13 × 104 UFP/ml (Tabla 2).
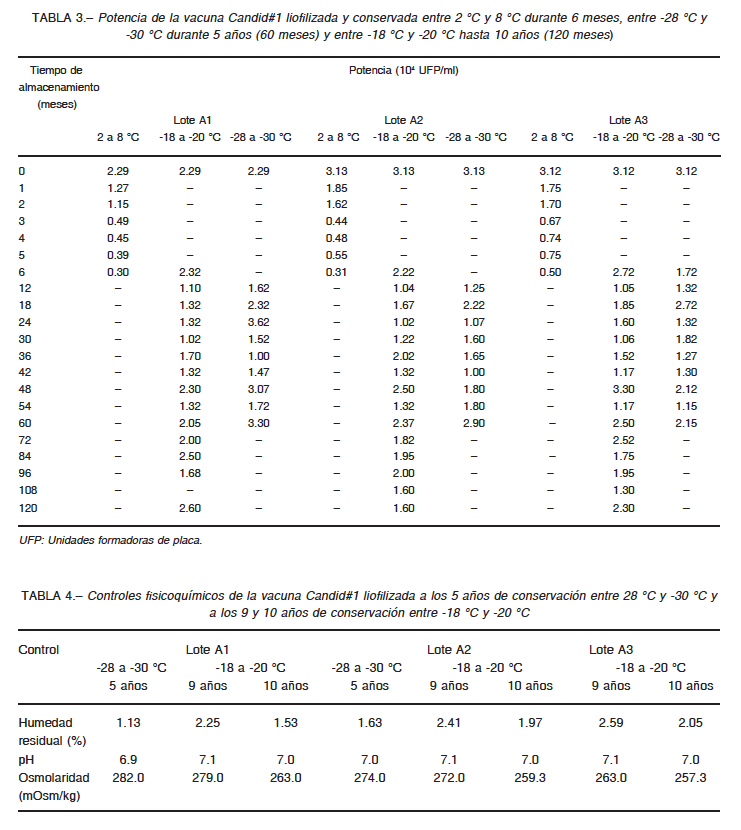
La potencia de la vacuna liofilizada conservada entre 2 °C y 8 °C se mantuvo entre 1.15 × 104 y 3.13 × 104 UFP/ml
durante dos meses. A partir del tercer mes, la potencia disminuyó a valores por debajo de la especificación para Candid#1 (< 1.00 x 104 UFP/ml) (Tabla 3).
La vacuna liofilizada conservada entre -18 °C y -20 °C mantuvo títulos virales por encima de 1.02×104 UFP/ml durante los 10 años del estudio (Tabla 3). El pH y la humedad residual también se mantuvieron dentro de valores aceptables (Tabla 4). La osmolaridad se mantuvo dentro del rango de la especificación del producto hasta los 9 años, pero a los 10 años descendió a valores inferiores a 260 mOsm/kg en dos de los tres lotes estudiados (Tabla 4).
La vacuna liofilizada conservada entre -28 °C y -30 °C mantuvo el título de virus entre 1.00 × 104 y 3.62 × 104 UFP/ml durante 5 años (Tabla 3), tiempo que estuvo almacenada según las indicaciones de los desarrolladores del producto, manteniendo el pH, la humedad residual y la osmolaridad dentro del rango de la especificación del producto (Tabla 4).
Discusión
En el desarrollo de inmunógenos, y de medicamentos en general, uno de los objetivos centrales es obtener una preparación eficaz que pueda llegar a cada población blanco con sus propiedades intactas. Para ello, los estudios de estabilidad miden el efecto de los factores fisicoquímicos, biofarmacéuticos y biológicos, y las condiciones ambientales (humedad, temperatura, oxígeno, luz, entre otras) sobre los principios activos durante la elaboración, el almacenamiento, el transporte y la utilización de los productos médicos. En el caso de la vacuna de virus Junín vivo atenuado Candid#1, la temperatura a la que se expone el producto durante las etapas mencionadas es de importancia decisiva dada la termolabilidad del virus Junín, característica común a todos los arenavirus.
En este trabajo se presentan los resultados de la exposición de Candid#1 como producto terminado (liofilizado y reconstituido) a diferentes temperaturas durante variables períodos de tiempo, como parte de un plan integral de estudio de su estabilidad. Los primeros ensayos consistieron en determinar la temperatura de almacenamiento del producto terminado (vial de diez dosis) en la planta de producción, para lo cual se utilizaron cámaras a -28 °C a -30 °C siguiendo las indicaciones de los desarrolladores del producto. Las determinaciones de la potencia y otros parámetros realizadas durante 5 años demostraron que en esas condiciones la vacuna mantenía intactas sus propiedades. Simultáneamente, se realizaron estudios a temperatura de refrigerador (2 °C a 8 °C) para fijar las condiciones de uso de Candid#1 en los vacunatorios, determinándose que esta vacuna puede ser mantenida reconstituida en estas condiciones durante 12 horas. Como producto liofilizado, Candid#1 puede ser almacenada en refrigerador durante 60 días.
Esos resultados representaron desafíos para la implementación de las campañas de vacunación con Candid#1, ya que el almacenamiento prolongado de la vacuna debía realizarse entre -28 °C y -30 °C, condiciones difíciles de lograr en los ambientes rurales donde se la administra. Para abordar estas dificultades, se analizó la posibilidad de utilizar freezers de tipo doméstico (-18 °C a -20 °C) para la conservación de Candid#1 en los centros de vacunación. Las determinaciones anuales de los diferentes parámetros demostraron que el producto mantuvo el título de virus original durante todos los diez años que duró el período de observación y solo su osmolaridad redujo por debajo de los valores especificados el décimo año de almacenamiento.
Durante el desarrollo de Candid#1 se determinó que la forma liofilizada sería la más conveniente para lograr la estabilidad prolongada del producto, ya que este proceso reduce el potencial daño al virus Junín causado por hidrólisis, agregación, desnaturalización, degradación y fluctuación del pH, los riesgos habituales de las presentaciones líquidas. También se especuló con la posibilidad de conservar esta vacuna a temperatura de refrigerador (2 °C a 8 °C) como ocurre con otros inmunógenos10. Los resultados indicaron que solo se puede almacenar Candid#1 liofilizada en estas condiciones durante 60 días, mientras que la misma presentación puede ser almacenada durante 9 años entre -18 °C y -20 °C. Estos resultados demuestran que la vacuna Candid#1 es un producto de muy prolongada estabilidad, que la temperatura de almacenamiento es el factor determinante de su vida útil y que, por consiguiente, la supervisión de la cadena de frío de esta vacuna es de fundamental importancia. La presentación de los resultados aquí descriptos ante la autoridad regulatoria nacional dio lugar a la Disposición ANMAT N° 1687 (Febrero 2017) en la que se aprueba un período de 9 años como vida útil de la vacuna Candid#1 liofilizada conservada entre -18 °C y -20 °C.
Agradecimientos: A los técnicos de cultivos celulares y control de calidad y a la Srta. Natalia Giovannoni por su ayuda en la compaginación del trabajo.
Conflicto de intereses: Ninguno para declarar
Bibliografía
1. Arribalzaga RA. Una nueva enfermedad epidémica a germen desconocido: hipertermia nefrótica, leucopénica y enantemática. Dia Med 1955; 27: 1204-10.
2. Parodi AS, Geenway DJ, Rugiero HR, et al. Sobre la etiología del brote epidémico de Junín. Dia Med 1958; 30: 2300-1.
3. Enria DA, Barrera Oro JG. Junin virus vaccines. In: Oldstone M.B.A., eds. Arenaviruses II. Current Topics in Microbiology and Immunology, vol 263. Berlin, Heidelber: Springer, 2002.
4. Department of Health and Human Services, Food and Drug Administration. The Orphan Drug Act, EE.UU. En: http://www.fda.gov/orphan/oda.htm; consultado marzo 2010.
5. Ambrosio AM, Saavedra MC, Riera LM, Fassio RM. La producción nacional de vacuna a virus Junín vivo atenuado (Candid #1) anti-fiebre hemorrágica argentina. Acta Bioquim Clin Latinoam 2006; 40: 5-17.
6. Ambrosio AM, Saavedra MC, Mariani MA, Gamboa G, Maiza AS. Argentine Hemorrhagic Fever Vaccines. Hum Vaccin 2011; 7: 694-700.
7. Ambrosio AM, Saavedra MC. La vacuna Candid#1 para prevenir la fiebre hemorrágica argentina. Perspectivas de la producción nacional. En: Temas de Zoonosis V. Basualdo J, Cachione R, Durlach R, Martino P, Seijo A, eds. Buenos Aires: Asociación Argentina de Zoonosis, 2011, p 37-41.
8. Disposición ANMAT N° 5812: Estudio clínico puente, en fase III, en voluntarios humanos sanos, de entre 15 y 65 años de edad, de ambos sexos, a riesgo de adquirir FHA, aleatorio, a doble ciego, para evaluar la comparabilidad entre la vacuna Candid#1 producida en la Argentina y la producida en Estados Unidos, 23 de septiembre de 2004. En: http://www.msal.gob.ar/dicei/index.php/institucional/marco-legal/368-resolucion-482007; consultado marzo 2016.
9. Enria DA, Ambrosio AM, Briggiler AM, Feuillade MR, Crivelli E, y grupo de estudio de la vacuna contra la Fiebre Hemorrágica Argentina. Vacuna contra la Fiebre Hemorrágica Argentina Candid#1 producida en la Argentina. Inmunogenicidad y seguridad. Medicina (B Aires) 2010; 70: 215-22.
10. Comité de Expertos de la OMS en Especificaciones para las Preparaciones Farmacéuticas. Informe 34. Anexo 5. Directrices para las pruebas de estabilidad de productos farmacéuticos que contienen sustancias medicamentosas bien establecidas en formas farmacéuticas corrientes. OMS, Ginebra, 1996.
11. Vacunación segura: cadena de frio “Manual de almacenamiento de las vacunas para el nivel operativo”. Programa nacional de control de enfermedades inmunoprevenibles. Manual CDF:1-40, Ministerio de Salud de la Nación 15/02/2013. En: http://www.msal.gob.ar/images/stories/bes/graficos/0000000441cnt-2013-07_manual-cadena-frio-cdf15x15_imprenta.pdf; consultado marzo 2014.
12. Disposición ANMAT N° 2819/2004. Bs. As., 18/5/2004. En: http://www.anmat.gov.ar/webanmat/Legislacion/Medicamentos/Disposicion_2004_2819.pdf; consultado junio 2005.
13. Code of Federal Regulations. Title 21, Part 610, Volume 7. Revised as of April 1, 2013. En: http://www.bpis.or.kr/wp-content/uploads/oldfile/regdata/FDA046-Part%20610.%20GENERAL%20BIOLOGICAL%20PRODUCTS%20STANDARDS.pdf; consultado abril 2014.
14. Westgard JO, Barry PL,Hunt MR. A multi-rule Shewhart chart for quality control in clinical chemistry. Clin Chem 1981; 27: 493-501.
15. Shewhart WA. Economic quality control of manufactured product. Bell System Technical Journal 1930; 9: 364-89.
1941
A good rule for writers: do not explain overmuch,
Una buena regla para escritores: no explique demasiado.
William Somerset Maugham (1874-1965)
