Resumen El estado de mal epiléptico (EME) es la emergencia más frecuente en la neuropediatría. Es el re-
sultado de un fallo en los mecanismos responsables de terminar la convulsión o de la iniciación de mecanismos que provocan una convulsión anormalmente prolongada. Esta definición se relaciona con el momento de iniciar el tratamiento. En general, el primer punto de tiempo o t1, es el momento cuando el tratamiento debería comenzarse, que es a los 5 minutos para las convulsiones tónico-clónicas generalizadas y a los 10 minutos para las focales con o sin compromiso de la conciencia. El segundo punto de tiempo o t2 marca el momento en el cual el daño neuronal o de las redes neuronales puede comenzar e indica que el EME debería ser controlado, que para los casos de mal tónico-clónico generalizados debe ser de 30 minutos. Todos los protocolos de tratamiento diferencian estadios en donde se utilizan diferentes fármacos: temprano o 1, establecido o 2, refractario o 3, súper-refractario o 4; y enfatizan el rápido reconocimiento y tratamiento de la actividad epiléptica persistente en cada estadio con el objetivo de reducir la morbimortalidad y las secuelas a largo plazo (después de t2).
Palabras clave: estado de mal epiléptico, pediatría, antiepilépticos, epilepsia
Abstract Status epilepticus. Status epilepticus (SE) is one of the most common neurologic emergencies in
pediatrics. It is a condition resulting either from the failure of the mechanisms responsible for seizure termination or from the initiation of mechanisms, which leads to abnormally, prolonged seizures. This definition provides a good guidance, when emergency treatment must be considered. In general, time point t1 is the time when treatment should be started, which is at 5 minutes for generalized tonic-clonic seizures, and at 10 min for focal seizures with or without impairment of consciousness. Time-point t2 marks the time at which neuronal damage or self-perpetuating alteration of neuronal networks may begin and indicates that SE should be controlled latest by that time; 30 min in case of generalized tonic-clonic seizures. All treatment protocols recognize a staged approach to treatment with different drugs used in early (stage I), established (stage II), refractory (stage III) and super-refractory SE (stage IV); and emphasize prompt recognition and treatment of persisting seizure activity at each stage aiming to reduce morbidity, mortality, and long-term consequences of status epilepticus (beyond t2).
Key words: status epilepticus, pediatrics, antiepileptic drugs, epilepsy
e-mail: mariabuompadre@gmail.com
El estado de mal epiléptico (EME) es la emergencia más frecuente en neuropediatría. Se describen al menos 20 episodios de EME convulsivo por 100 000 niños por año1 y en uno de cada ocho pacientes (12%) es el modo de debut de su epilepsia. El EME convulsivo en pediatría se asocia con una mortalidad a corto plazo de hasta el 3% y a largo plazo del 7% aproximadamente2. En aquellos que superan el EME convulsivo, frecuentemente se documentan secuelas funcionales, neurocognitivas y reducción en la calidad de vida2. El EME puede no solo ser la expresión más grave de una epilepsia, sino también la consecuencia de una agresión aguda cerebral o sistémica que conduce a una excesiva hiperexcitación del tejido nervioso.
Definición y evolución en el concepto
El EME, considerado como la forma más extrema de una convulsión, fue incluido en la clasificación de convulsiones de la Liga Internacional contra la Epilepsia (ILAE) de 1970 y 19813, 4. En 1970, se lo definió como la convulsión que persiste por un período suficiente o se repite lo necesario como para producir una condición persistente. El EME se dividió en parcial, generalizado o unilateral, básicamente reproduciendo la clasificación de convulsiones3. En la revisión de 1981, la definición se modificó mínimamente a convulsión que persiste por un período suficiente o se repite frecuentemente como para que no exista recuperación entre los ataques4. Estos conceptos, aunque de gran valor, no definían la duración de la convulsión (tiempo suficiente) ni tampoco se incluía la semiología. Debido a que las propuestas por la ILAE no precisaban la duración del EME, fueron publicadas múltiples definiciones operacionales. Meldrum y col.5 sugirieron que una convulsión de 82 minutos o más en babuinos podía causarinjuria neuronal irreversible. Esta observación condujo a la definición comúnmente utilizada de EME como una convulsión de 30 minutos de duración6. La lógica detrás de esta definición fue que la injuria neuronal irreversible aparecía luego de los 30 minutos.
Lowenstein y col. propusieron una definición operacional, aplicable principalmente a EME convulsivo generalizado, como convulsiones continuas por más de 5 minutos, considerando que si persisten > 5 minutos es probable que continúen > 30 minutos, siendo estas últimas más difíciles de tratar y recalcando la importancia del tratamiento precoz para evitar la progresión hacia estadios refractarios y sus secuelas7.
La ILAE (2015) lo define como la condición que resulta de un fallo en los mecanismos responsables de terminar la convulsión o de la iniciación de mecanismos que provocan una convulsión anormalmente prolongada. Es una condición que puede provocar consecuencias a largo plazo, que incluyen muerte e injuria neuronal y alteraciones en la red neuronal8. Esta nueva definición de EME se relaciona con el momento para iniciar el tratamiento. En general, el primer punto de tiempo o t1, es cuando el tratamiento debería comenzarse, que es a los 5 minutos para las convulsiones tónico-clónicas generalizadas y a los 10 minutos para las focales con o sin compromiso de la conciencia. El segundo punto de tiempo o t2 marca el momento en el cual el daño neuronal o de las redes neuronales puede comenzar e indica que el EME debería ser controlado, que para los casos de mal tónico-clónico generalizados debe ser de 30 minutos9. Podría considerarse que el t2 en los estados convulsivos focales con compromiso de la conciencia, sea de 60 minutos.
Clasificación del estado de mal epiléptico
La ILAE también propuso una nueva clasificación, formada por 4 ejes8:
1. Semiología
2. Etiología
3. Correlato en el EEG
4. Edad
Idealmente, cada paciente debería ser categorizado en cada uno de los 4 ejes. Sin embargo, no siempre es posible. Al debut, es factible determinar la edad del paciente y la semiología de las convulsiones. La etiología puede llevar tiempo para identificarla y el registro electroencefalográfico puede no estar disponible al inicio. Sin embargo, el EEG influirá en la elección y agresividad del tratamiento, pronóstico y abordaje clínico, por lo que debe ser realizado cuando sea posible. De hecho, algunas formas de EME pueden ser solo diagnosticadas con el EEG. Al igual que en otros desórdenes neurológicos agudos, la semiología (síntomas y signos) y el patrón electroencefalográfico en el EME son extremadamente dinámicos y pueden variar en un corto período. Por lo tanto, el examen neurológico repetido y el EEG en un paciente con EME pueden conducir a una diferente clasificación. Por ejemplo, el EME puede comenzar con síntomas motores focales evolucionando a un EME bilateral convulsivo y horas más tarde a un EME no convulsivo con coma o mínimos signos motores. Asimismo, el EEG puede mostrar descargas periódicas lateralizadas al comienzo y un patrón de sincronías bilaterales en un segundo registro.
Eje 1: Semiología
Se refiere a la presentación clínica del EME y por lo tanto es el esqueleto de esta clasificación. Las diferentes formas clínicas de EME se diferencian a través de dos criterios taxonómicos: actividad motora y compromiso de la conciencia, definiendo dos grupos principales10: (a) EME con síntomas motores notorios (o prominentes) que incluye todas las formas convulsivas y (b) aquellos sin síntomas motores notorios que representan las formas no convulsivas de EME. El EME no convulsivo (EMENC) comatoso es una condición potencialmente fatal que requiere tratamiento urgente, mientras que el EME no convulsivo sin coma ocurre en las formas de EME de ausencia o el focal con compromiso de la conciencia8. Dentro de las formas con síntomas motores notorios se incluyen el tónico clónico generalizado, el mioclónico (con y sin coma), el motor focal donde se incluye la epilepsia parcial continua, el tónico y el hiperquinético. Dentro de las formas sin síntomas notorios prominentes o EMENC se describen: el EMENC con coma (EME sutil), el EMECNC sin coma que puede ser generalizado (como en los de las ausencias típicas o atípicas, o con mioclónicas), focal o desconocido (autonómico)8.
Eje 2: Etiología
La etiología subyacente del EME está categorizada de manera consistente con los conceptos de la propuesta de la ILAE (2010). Se describen 2 grupos: (i) conocida o sintomática y (ii) desconocida o criptogénica11. Conocida o sintomática: puede ser estructural, metabólica, infecciosa, inflamatoria, tóxica o genética. Basada en su relación temporal se subdivide en aguda, remota y progresiva. El término “idiopático” o “genético” no se aplica como causa subyacente del EME. En los síndromes epilépticos idiopáticos o genéticos, la causa del estado no es la misma que la enfermedad, pero algunos factores tóxicos, metabólicos o intrínsecos (como la deprivación del sueño) pueden desencadenar el EME. Un accidente cerebrovascular o una encefalitis pueden ser la causa aguda (sintomática) de un EME.
Eje 3: Correlato electroencefalográfico
Ninguno de los patrones ictales en el EEG, en cualquiera de los tipos de EME, es específico. Las descargas epileptiformes son consideradas como distintivas, pero cuando la duración del EME aumenta, los cambios en el EEG y los patrones rítmicos no epileptiformes pueden prevalecer. Patrones electroencefalográficos similares, tales como las ondas trifásicas, pueden registrarse en varias enfermedades. El registro electroencefalográfico afectará la elección y la agresividad del tratamiento, el pronóstico y el abordaje clínico, por lo que se recomienda realizarlo rápidamente. De hecho, algunas formas solo serán reconocibles con el registro electroencefalográfico.
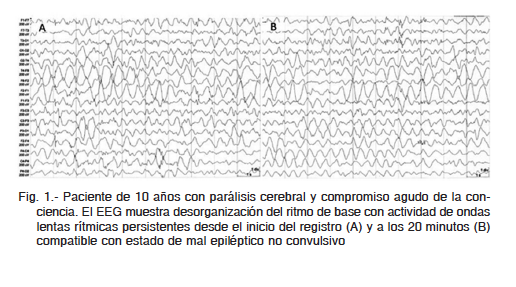
En las formas no convulsivas del EME es imprescindible el registro electroencefalográfico para su diagnóstico (Fig. 1). En las formas más extremas, donde el paciente está en coma profundo, solo el EEG puede revelar descargas epileptiformes o rítmicas que permiten el diagnóstico12,13. La ILAE recomienda utilizar los criterios electroencefalográficos para EME no convulsivo de Salzburg13. Basados en consensos y series descriptivas se propone esta terminología para describir los patrones de EEG en el EME:
Localización: generalizado (incluyendo los patrones sincrónicos bilaterales), lateralizado, bilateral independiente y multifocal
Nombre del patrón: descargas periódicas, actividad delta rítmica de ritmos delta o espiga/onda y otros tipos
Morfología: número de fases, amplitud y polaridad
Características temporales: prevalencia, frecuencia, duración; duración del patrón, comienzo (abrupto vs. gradual) y dinámica (creciente, fluctuante o estático)
Modulación: inducida por estímulos vs. espontánea
Efecto de la intervención (fármacos) en el EEG8
Eje 4: Edad
Se diferencia en neonatales (o a 30 días), lactantes (1 mes a 2 años), preescolares y escolares (> 2 años a 12 años), adolescentes y adultos (> 12 años a 59 años) y adultos mayores (≥ 60 años)8.
Fisiopatología
Fase bioquímica del EME
Las convulsiones son el resultado de una alteración entre el balance normal de los procesos excitatorios e inhibitorios. Las descargas hipersincrónicas neuronales son mediadas principalmente por glutamato y los canales voltaje-dependientes de sodio y de calcio. La terminación de una convulsión depende de los efectos inhibitorios de los receptores de GABA activados y de los canales voltaje-dependiente de potasio. Luego del comienzo, el fracaso de los mecanismos intrínsecos o la disrupción de la inhibición por factores extrínsecos, conducirá a una actividad epiléptica prolongada. La fase mantenida del EME se caracteriza por internalización sináptica de los receptores GABA y expresión de los receptores de NMDA y de alfa-amino-3-hidroxi-5-metil-4-ácido isoxipropionico, provocando convulsiones refractarias a los fármacos antiepilépticos. En el período posterior, el EME continúa debido al aumento de la expresión de neuropéptidos proconvulsivos y disminución de los inhibitorios. Poco se conoce de los cambios bioquímicos asociados con las etapas refractarias y súper-refractarias del EME. En un período de horas a semanas, los cambios a largo plazo en la expresión de genes pueden ocurrir de forma secundaria, provocando reorganización neuronal14.
Injuria neuronal y muerte
La muerte celular ocurre aun en ausencia de hipoxia, acidosis, hipoglucemia y otros factores de confusión y puede ser mediada por la “necrosis programada” y apoptosis. Se ha demostrado en humanos que la enolasa sérica, un biomarcador de injuria neuronal, aumenta en el EME; mientras que en la anatomía patológica se ha descripto
disminución de la densidad de neuronas en el hipocampo post mortem. También podría depender del tipo de convulsión y de la etiología. El EME de ausencias y el EMENC en pacientes con epilepsia subyacente pueden ser menos propensos a la injuria, mientras que el EME focal complejo se asocia más con cambios patológicos14.
Etapas fisiológicas del EME
En las etapas tempranas compensadas, las convulsiones se acompañan de activación simpática significativa. Durante esta etapa, se observa hipertensión, incremento del gasto cardíaco y del flujo sanguíneo cerebral. Además, se observa aumento del ácido láctico y de la glucosa. Luego de una actividad convulsiva prolongada (> a 30 minutos) se produce una descompensación caracterizada por pérdida de la autorregulación cerebral, disfunción cardiovascular y signos de crisis metabólica sistémica como hipoxia, hipoglucemia y acidosis. Los fallos en prevenir estos desordenes fisiológicos puede exacerbar el daño neuronal asociado al EME refractario14.
Epidemiología
En la serie prospectiva más amplia de pacientes con EME, la mayor frecuencia corresponde a menores de 1 año, luego 1-4 años, descendiendo posteriormente y con un alza en adultos15,16 . En EME súper-refractario no existen estudios controlados, estimándose una frecuencia de 10-15% de los EME que se hospitalizan. Se ha comunicado que >50% de los EME refractarios que requieren anestesia, evolucionan a la etapa súper-refractaria, y que 20% recurre dentro de los 5 días de reducción de la anestesia17. Aránguiz y col.18 publicaron una serie de 41 niños con EME, destacando que 56% se presentó en < 2 años, 58% eran epilépticos en tratamiento y la etiología más frecuente fue sintomática aguda. De los niños previamente sanos, el 96% evolucionó con secuelas neurológicas, sin diferencias entre EME y el EMENC. La recurrencia es más frecuente en niños que en adultos19. En niños con epilepsia sintomática, los principales factores de riesgo para desarrollar EME son: alteraciones electroencefalográficas focales, presencia de crisis focales secundariamente generalizadas, EME como debut de la epilepsia y patología en la neuroimagen20.
Formas clínicas
– Estado de mal epiléptico convulsivo generalizado
– Estado de mal epiléptico tónico-clónico. Tiene mayor incidencia en edades extremas de la vida. Se asocia con mayor gravedad debido a las complicaciones sistémicas, dependiendo de la duración. La morbilidad publicada es muy amplia, desde alteraciones cognitivas y neurológicas hasta epilepsia. Son crisis tónico-clónicas generalizadas o bien de inicio parcial con generalización secundaria. Si se deja evolucionar, desaparecen las convulsiones, el paciente entra en coma y el diagnóstico solo puede efectuarse con la ayuda del EEG21.
– Estado de mal epiléptico convulsivo tónico. Es menos frecuente que el EME tónico-clónico o clónico y se presenta casi exclusivamente en los pacientes con síndrome de Lennox-Gastaut. Puede ser desencadenado por la administración de benzodiacepinas endovenosas como el diazepam y clonazepam o por la administración vía oral de clonazepam. Los episodios de EME tónico pueden ser prolongados (Fig. 2) y a medida que los episodios se repiten, el fenómeno tónico es menos manifiesto pero se agregan crisis autonómicas (aumento de la frecuencia cardíaca, de las secreciones o de la frecuencia respiratoria). También pueden asociarse crisis de ausencias o periodos confusionales22.
– Estado de mal epiléptico convulsivo clónico. Se caracteriza por contracciones musculares clónicas que se repiten de forma arrítmica y asimétrica. Afecta a los niños pequeños.
– Estado de mal epiléptico convulsivo mioclónico. Se caracteriza por la repetición de crisis mioclónicas masivas. Ocurre en pacientes con epilepsia mioclónica juvenil, epilepsias mioclónicas en niños, epilepsia con mioclonías palpebrales con ausencias o sin ellas y en otras epilepsias generalizadas idiopáticas con crisis de ausencias y tónico-clónicas. El paciente puede conservar la conciencia. También puede presentarse en las epilepsias mioclónicas progresivas, síndrome de Dravet, epilepsia mioclónica-astática y síndrome de Lennox-Gastaut. El EME asociado a mioclonías negativas se documentó en pacientes con epilepsias focales y bisincronías bilaterales secundarias, en especial en las formas idiopáticas y en las secundarias por polimicrogiria unilateral o multilobular. Se presentan con caídas frecuentes, marcha inestable, menor iniciativa motora o cambio de lateralidad. El EEG, especialmente con poligrafía, es de suma importancia22.
– Estado de mal epiléptico convulsivo focal. El EME convulsivo focal motor puede presentarse en una encefalopatía aguda o en una epilepsia. En los EME puramente focales puede existir compromiso de la conciencia y síntomas autonómicos. Cuando las mioclonías focales o segmentarias combinadas con convulsiones focales persisten durante varios días o meses, corresponden a crisis parciales continuas, manifestación distintiva del síndrome de Kojewnikow, que puede asociarse con lesiones no progresivas22.
– Estado de mal epiléptico no convulsivo generalizado. Está definido por el compromiso de la conciencia, que va desde un simple enlentecimiento hasta la pérdida total de la misma, asociado a descargas bilaterales de complejos de punta-onda23. La forma de EME no convulsivo de ausencias atípicas en el contexto de síndrome de Lennox-Gastaut o de epilepsias generalizadas secundarias, es

más frecuente que el EME no convulsivo de ausencias típicas asociadas con epilepsia-ausencia de la niñez. Los síntomas pueden ser solo un compromiso mínimo de la conciencia, por lo cual el paciente puede continuar con actividades automáticas de la vida diaria. Puede haber automatismos complejos y episodios de fuga. En el 50% de los casos se presentan manifestaciones motoras asociadas, como mioclonías o crisis atónicas. El pronóstico depende del síndrome epiléptico subyacente.
– Estado de mal epiléptico no convulsivo focal. Es la forma más común en los adultos22. El compromiso de la conciencia diferencia al EME no convulsivo focal complejo del simple. Pueden ocurrir situaciones intermedias, desde un cuadro confusional grave hasta una mínima confusión o episodios prolongados de crisis parciales (miedo, pérdida de visión, conductas psicóticas, manifestaciones autonómicas, etc.). El EME no convulsivo autonómico es más frecuente en los niños con síndrome de Panayiotopoulos24. Alrededor del 50% de los niños con este síndrome pueden presentarlo y debe diferenciarse de encefalopatías agudas secundarias a tóxicos, encefalitis o accidente cerebrovascular, entre otros. La identificación de esta forma de estado de mal es crucial para evitar estudios y tratamiento agresivos.
Tratamiento del estado de mal epiléptico
La evidencia es limitada en el tratamiento farmacológico del EME. Está demostrado que la intervención precoz puede modificar el pronóstico de los pacientes25 ya que se asocia con menor morbimortalidad, menor cantidad de fármacos requeridos en la hospitalización y reducción de la duración de las convulsiones.
Todos los protocolos de tratamiento diferencian estadios en donde se utilizan diferentes fármacos: temprano o 1, establecido o 2, refractario o 3, súper-refractario o 4, y enfatizan el rápido reconocimiento y tratamiento de la actividad epiléptica persistente en cada estadio con el objetivo de reducir la morbimortalidad y las secuelas a largo plazo del EME (después de t2). En el estadio temprano las benzodiacepinas endovenosas son las más efectivas ya que son capaces de controlar el EME en casi dos tercios de todos los pacientes. Su efecto favorece al inhibidor de los neurotransmisores1. Las más comúnmente utilizadas son el lorazepan, diazepam, midazolam y clonazepam. En el estadio establecido se utilizan fármacos endovenosos (EV) como la fenitoína, fenobarbital, levetiracentan, valproato y lacosamida; sin embargo, no existe evidencia clase I para elegir uno sobre el otro26.
En adultos, se ha demostrado que la eficacia de dosis repetidas de fármacos antiepilépticos de segunda línea disminuye: el 56% responde a la primera línea de tratamiento, el 7% responde a la segunda línea y el 2.3% a otro fármaco antiepiléptico no anestésico1.
En el estadio refractario se utilizan frecuentemente las drogas anestésicas endovenosas (tiopental, midazolam, propofol). La infusión continua de midazolam es una de las elecciones más frecuentes, seguida por el propofol y los barbitúricos27-29. En el estado súper-refractario, cuando el tratamiento con un fármaco anestésico EV por más de 24 horas falla en el control del EME, se alcanza la etapa de EME súper-refractario o EME maligno29. Las recomendaciones se basan exclusivamente en series de casos e incluyen diferentes opciones de tratamiento como la ketamina, los esteroides, el magnesio, la gammaglobulina EV, la dieta cetogénica, la neuroestimulación y en algunos casos con lesión demostrada, la neurocirugía.
Evolución
La mortalidad a corto plazo del EME alcanza hasta el 8% en UCI, directamente relacionada con la causa, siendo hasta 2% por el EME, y entre 12 y 16% secundaria a la causa aguda. En este grupo la cifra se eleva hasta 22% en menores de 2 años. La morbilidad a largo plazo incluye discapacidad cognitiva, déficit neurológico, daño hipocampal, epilepsia (13-74%), principalmente de origen focal30. Para el EME súper-refractario, Shorvon describe 35% de mortalidad, 13% de daño neurológico leve y 13% grave, y recuperación a la condición de base en 35%. No existen datos epidemiológicos en población infantil.
Conflicto de intereses: Ninguno para declarar
Bibliografía
1. Tully I, Draper ES, Lamming CR, et al. Admissions to paediatric intensive care units (PICU) with refractory convulsive status epilepticus (RCSE): A two-year multi-centre study. Seizure 2015; 29: 153-61.
2. Sánchez Fernández I, Abend N, Agadi A, et al. Time from convulsive status epilepticus onset to anticonvulsant administration in children. Neurology 2015; 84: 2304-11.
3. Gastaut H. Clinical and electroencephalographical classification of epileptic seizures. Epilepsia 1970; 11: 102-13.
4. Proposal for revised clinical and electroencephalographic classification of epileptic seizures. From the Commission on Classification and Terminology of the International League Against Epilepsy. Epilepsia 1981; 22:489-501.
5. Meldrum BS, Horton RW. Physiology of status epilepticus in primates. Arch Neurol 1973; 28: 1-9.
6. Guidelines for epidemiologic studies on epilepsy. Commission on Epidemiology and Prognosis, International League Against Epilepsy. Epilepsia 1993; 34: 592-6.
7. Lowenstein DH, Bleck T, Macdonald RL. It’s time to revise the definition of status epilepticus. Epilepsia 1999; 40:120-2.
8. Trinka E, Cock H, Hesdorffer D, et al. A definition and classification of status epilepticus-report of the ILAE task force on classification of status epilepticus. Epilepsia 2015; 56: 515-23.
9. Trinka E, Kälviäinen R. 25 years of advances in definition, classification and treatment of status epilepticus. Seizure 2017; 44:65-73.
10. Betjemann JP, Lowenstein DH. Status epilepticus in adults. Lancet Neurol 2015; 14: 615-24.
11. Trinka E, Hofler J, Zerbs A. Causes of status epilepticus. Epilepsia 2012; 53: 127-38.
12. Bauer G, Trinka E. Nonconvulsive status epilepticus and coma. Epilepsia 2010; 51: 177-90.
13. Trinka E, Leitinger M. Which EEG patterns in coma are nonconvulsive status epilepticus? Epilepsy Behav 2015; 49: 203-22.
14. Poblete R, Sung G. Status epilepticus and beyond: a clinical review of status epilepticus and an update on current management strategies in super-refractory status epilepticus. Korean J Crit Care Medicine 2017; 32: 89-105.
15. Chin R, Neville B. Treatment of community-onset, childhood convulsive status epilepticus: a prospective, population-based study. Lancet Neurol 2008; 7: 696-703.
16. Riviello J Jr, Ashwal S, Hirtz D, et al. Practice parameter: diagnostic assessment of the child with status epilepticus (an evidence-based review): Report of the Quality and the Practice Committee of the Child Neurology Society Standards Subcommittee of the American Academy of Neurology. Neurology 2006; 67: 1542-50.
17. Shorvon S, Ferlisi M. The outcome of therapies in refractory and super-refractory convulsive status epilepticus and recommendations for therapy. Brain 2012; 135: 2314-28.
18. Aránguiz J, Hernández M, Escobar RG, Mesa T. Estado epiléptico infantil en un hospital universitario: estudio descriptivo. Rev Neurol 2008; 47: 286-90.
19. Chin RF, Neville BG, Scott RC. A systematic review of the epidemiology of status epilepticus. Eur J Neurol 2004; 11: 800-10.
20. Novak G, Maytal J, Alshansky A, Ascher C. Risk factors for status epilepticus in children with symptomatic epilepsy. Neurology 1997; 49: 533-7.
21. Lowenstein DH, Aminoff MJ. Clinical and EEG features of status epilepticus in comatose patients. Neurology 1992; 42: 100-4.
22. Caraballo R, Fejerman N. Tratamiento de las epilepsias. Buenos Aires: Editorial Panamericana, 2009.
23. Caraballo R, Reyes Valenzuela G, Carpio Ruiz A. Estado de mal epiléptico no convulsivo. Rev Chilena Epilepsia 2015; 1: 5-11.
24. Ferrie C, Caraballo R, Covanis A, et al. Autonomic status epilepticus in Panayiotopoulos syndrome and other childhood and adult epilepsies: a consensus view. Epilepsia 2007; 48: 1165-72.
25. Madzar D, Geyer A, Knappe RU, et al. Association of seizure duration and outcome in refractory status epilepticus. J Neurol 2016; 263: 485-91.
26. Yasiry Z, Shorvon SD. The relative effectiveness of five antiepileptic drugs in treatment of benzodiazepine-resistant convulsive status epilepticus: A meta-analysis of published studies. Seizure 2014; 23: 167-74
27. Ferlisi M, Hocker S, Grade M, Trinka E, Shorvon S. International steering committee of the StEp A. Preliminary results of the global audit of treatment of refractory status epilepticus. Epilepsy Behav 2015; 49: 318-24.
28. Claassen J, Hirsch LJ, Emerson RG, Mayer SA. Treatment of refractory status epilepticus with pentobarbital, propofol, or midazolam: a systematic review. Epilepsia 2002; 43: 146-53.
29. Ferlisi M, Shorvon S. The outcome of therapies in refractory and superrefractory convulsive status epilepticus and recommendations for therapy. Brain 2012; 35: 2314-28.
30. Raspall-Chaure M, Chin R, Neville B. Outcome of paediatric convulsive status epilepticus: a systematic review. Lancet Neurol 2006; 5: 769-79.
